2018 год № 1
Хирургия
2Сибирский федеральный биомедицинский исследовательский центр имени академика Е.Н. Мешалкина, 630055, ул. Речкуновская, 15, г. Новосибирск
Резюме:
Ключевые слова:
2The Siberian Federal Biomedical Research Centre named after Academician E.N. Meshalkin, Novosibirsk
Summary:
Key words:
Введение |
 |
 |
В кардиохирургической практике в последние годы активно используются устройства и методы механической поддержки кровообращения (МПК), что позволяет выполнить в полном объеме операции при ремоделировании миокарда левого желудочка (ЛЖ). Применения систем Impella Recover Support System LD 5.0. дает возможность значительно минимизировать интраоперационную летальность и риск осложнений в момент отключения искусственного кровообращения (ИК) у больных с декомпенсированной хронической сердечной недостаточностью, малым сердечным выбросом, низкой фракцией выброса левого желудочка (ФВ ЛЖ) менее 30 % и дисфункцией правого желудочка (ПЖ) [1, 5, 6, 7].
Анализируя накопленный опыт использования транскатетерного микроаксиального насоса Impella RSS ®LP 5.0 (Abiomed, США) при завершении основного этапа оперативного вмешательства доступом через восходящую аорту в ЛЖ, следует отметить особое значение ультразвукового (УЗ) контроля на всех этапах позиционирования устройства. Чреспищеводная эхокардиография (ЧПЭхоКГ) используется перед имплантацией для оценки анатомических особенностей аорты и выходного тракта ЛЖ. Во время и после имплантации с помощью ЧПЭхоКГ проводится контроль корректного позиционирования системы, достижения максимальной производительности девайса, а также оценка систолической функции левого и правого желудочков, что обеспечивает профилактику интраоперационных осложнений [2, 3, 4].
Цель исследования - оценить эффективность интраоперационного УЗ пособия при использовании вспомогательного устройства МПК Impella RSS ®LP 5.0 больным с низким сердечным выбросом и ремоделированием миокарда ЛЖ.
Материалы и методы
|
 |
 |
В объеме предоперационной подготовки обследовано 28 больных ИБС, мужчины в возрасте от 59 до 72 лет. Все пациенты имели постинфарктный кардиосклероз (ПИКС), аневризматическую трансформацию передней стенки и верхушки ЛЖ, тяжелую застойную сердечную недостаточность ФК III-IV по NYHA, рефрактерную к лекарственной терапии.
Перед операцией и в послеоперационном периоде проводились исследования 3DTTE и МРТ в рамках контроля глобальной сократительной способности миокарда ЛЖ. Трем пациентам из обследованной группы выполнено оперативное вмешательство в объеме коронарного шунтирования, пластики аневризмы левого желудочка, пластики митрального клапана на опорном кольце и/или протезирование митрального клапана с использованием транскатетерного микроаксиального насоса Impella RSS ®LP 5.0. Интраоперационное УЗ пособие сопровождало все манипуляции перед имплантацией, во время имплантации системы обхода ЛЖ трансаортальным доступом и на этапе функционирования устройства.
В работе использовались диагностические системы УЗИ: System Philips iE33, Acuson X300PE и МРТ: Siemens Magnetom Аvanto 1,5Тл.
Статистический анализ проведен с помощью стандартных методов. Количественные данные представлены в виде медианы, 2,5-97,5-го процентилей, минимального и максимального значений. Достоверность различий оценивали с помощью критерия Манна - Уитни. Проведен корреляционный анализ с расчетом коэффициента ранговой корреляции Спирмена. Критерием достоверности считали p≤0,05.
Результаты и обсуждение
|
 |
 |
Применение дорогостоящих систем МПК оправдано у трех категорий больных [1, 6]. К первой группе относятся пациенты, которых после проведения операции на открытом сердце невозможно отключить от аппарата ИК (2-8 % пациентов). Ко второй группе относятся пациенты с острым поражением сердечной мышцы. В этом случае для преодоления периода возникшей острой декомпенсированной сердечной недостаточности (СН) необходима временная гемодинамическая поддержка. Вероятность восстановления нормальной деятельности сердца через определенный период времени в сочетании с интенсивной медикаментозной терапией достаточно высока [8, 9]. К третьей группе относятся пациенты с хроническими тяжелыми формами сердечной недостаточности [1, 7].
Разработанные в 1997 г. для операций на работающем сердце системы внутриаортального левожелудочкового обхода (ЛЖО) с помощью осевого насоса Impella RSS ®LP 5.0 находятся на этапе клинического внедрения. Администрация по контролю за продуктами питания и лекарствами США (FDA) в июне 2008 одобрила применение системы Impella в клиниках США [2, 5]. В клинических исследованиях PROTECT I и PROTECT II было продемонстрировано, что использование Impella 2,5 для поддержки гемодинамики при проведении ЧКВ у пациентов группы высокого риска позволило снизить количество осложнений, улучшить качество жизни, ускорить выписку из стационара, снизить частоту повторных процедур [9, 10, 11, 12].
Анатомическими препятствиями для использования обхода ЛЖ являются механические протезы АК, Стеноз и кальциноз АК с S менее 1,5 с м2, умеренная и выраженная недостаточность аортального клапана, расслаивающая аневризма аорты, окклюзии подвздошных артерий, гипертрофическая кардиомиопатия, SAM синдром, миксоматоз створок митрального клапана [5, 9].
Устройство представляет собой винтовой насос, перекачивающий кровь из левого или правого желудочка в восходящую аорту или ствол легочной артерии, имплантируемый трансаортальным и чрескожным пункционным доступом через бедренную артерию в левый желудочек. Достоинствами девайса Impella RSS ®LP 5.0 являются небольшие размеры, минимальная инвазивность, возможность эндоваскулярной доставки, а также способность поддерживать кровообращение до 6 часов, что позволяет улучшить коронарный кровоток, увеличить сердечный выброс, снизить потребление кислорода. Наряду с этим отмечается относительно низкий уровень гемолиза и сладжирования эритроцитов при "либеральном" антикоагулянтном режиме, достаточное пульсовое кровенаполнение периферических отделов сосудистой системы [5, 6, 7, 8].
На проксимальном конце канюли находится электронный сенсор измерения давления, генерирующий позиционный сигнал пропорциональный разнице давления в канюле и вне ее, который позволяет системе контроля определить правильность имплантации насоса. Когда система находится в корректной позиции, верхушка сенсора измеряет давление в аорте, а нижняя поверхность сенсора показывает давление в полости ЛЖ [5, 11].
Во время работы устройства МПК достигается определенный уровень производительности скорости потока крови от 0,3 до 5,5 л в минуту. Использованная в работе система Impella RSS®LP 5.0 позволяет перекачивать максимально до 5 л крови в минуту из полости ЛЖ в аорту. На первом этапе перед имплантацией девайса ТЕЕ используется для оценки анатомических особенностей выходного тракта левого желудочка, аортального клапана, синусов Вальсальвы, восходящей аорты. По окончании основного этапа оперативного вмешательства девайс имплантируется доступом через восходящую аорту в ЛЖ, где в месте имплантации к аорте подшивают линейный протез диаметром 10 мм, затем через протез в аорту и ЛЖ проводят систему. При этом особое значение имеет УЗ контроль позиционирования системы [1, 2, 3, 4].
После имплантации для получения адекватного позиционного сигнала проксимальная часть канюли должна выступать в полость ЛЖ на 4 см ниже створок аортального клапана (АК). Необходимое расстояние между створками АК и аортотомией должно составлять более 7 см. К сожалению, именно этот анатомический отдел визуализации, где происходит выброс крови из выходного отдела насоса, плохо контролируется как хирургами, так и специалистами ультразвуковой диагностики (рис. 1).
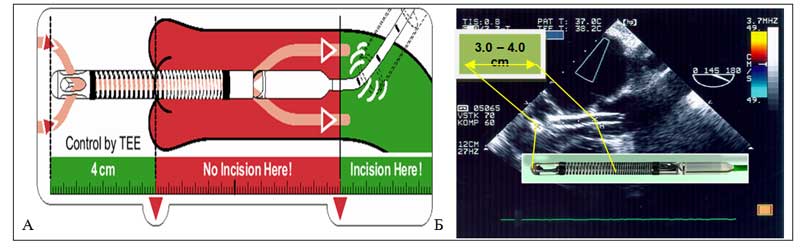
Рис. 1. Принципы позиционирования (А) и ультразвуковая визуализация правильного положения (Б) системы Impella RSS®LP 5.0
>Принято использовать режим цветного допплеровского картирования, как дополнительного способа определить корректность положения насоса. Если устройство находится в правильной позиции, мозаичный турбулентный кровоток визуализируется выше створок АК в области выхода канюли насоса, что отражает удовлетворительный позиционный сигнал, соответствующий циркулирующему объему крови 4-5 литров в минуту (рис. 2).
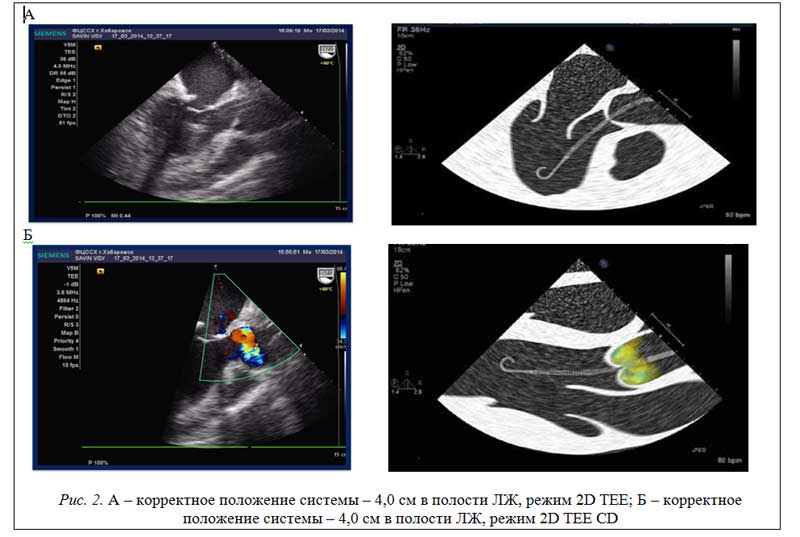
Рис. 2. A - корректное положение системы - 4,0 см в полости ЛЖ, режим 2D TEE; Б - корректное положение системы - 4,0 см в полости ЛЖ, режим 2D TEE CD
Если насос смещен слишком далеко в полость ЛЖ, основной объем крови будет выбрасываться под створками аортального клапана, что требует дополнительных усилий миокарда левого желудочка и пациент не получает всех преимуществ использования системы механической поддержки кровообращения (рис. 3).
Механическое повреждение эритроцитов о стенки выводного тракта ЛЖ способствует их гемолизу, что быстро проявляется в анализах мочи. В ситуации, когда насос находится слишком близко к створкам АК эффект тоже минимизирован поскольку объем крови застаивается в полости ЛЖ, кроме того, высок риск повреждения и блока передней створки митрального клапана (МК) [5].
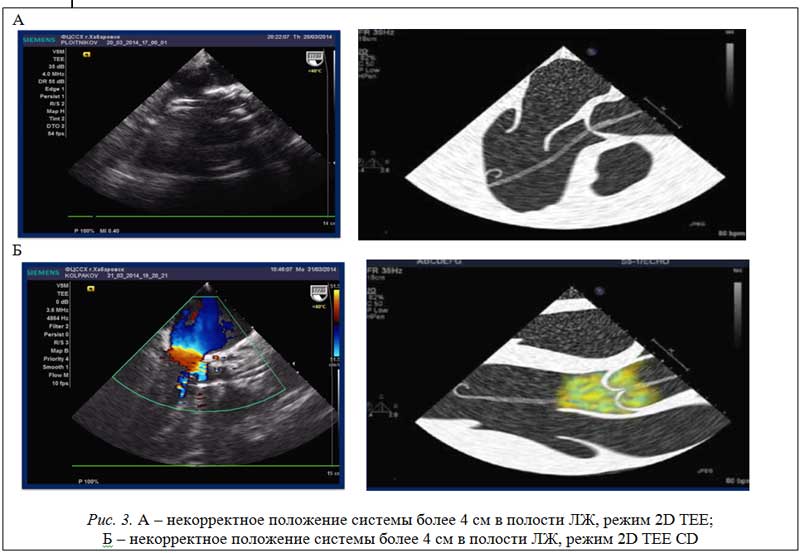
Рис. 3. A - некорректное положение системы более 4 см в полости ЛЖ, режим 2D TEE;
Б - некорректное положение системы более 4 см в полости ЛЖ, режим 2D TEE CD
В случае, когда насос находится слишком близко к створкам, папиллярным мышцам или субаннулярным структурам, окружающим МК, это может влиять на функцию МК и негативно сказаться на позиционном потоке системы. Если канюля касается папиллярных мышц, катетер может быть заблокирован в хордах МК, что увеличивает вероятность повреждения структур сердца и обструкции оттока крови из ЛЖ [3, 5].
В ФГБУ ФЦССХ г. Хабаровск получен опыт использования микроаксилярного насоса Impella RSS®LP 5.0 пациентам, имеющим постинфарктное ремоделирование миокарда левого желудочка, аневризматическую трансформацию верхушки ЛЖ, низкую ФВ ЛЖ и тенденцию к снижению функции ПЖ.
Методами трехмерной трансторакальной эхокардиографии (3DТТЭхоКГ) и магнитно-резонансной томографии (МРТ) перед операцией обследованы 28 больных в целях отбора для применения системы обхода левого желудочка. У всех наблюдаемых выявлены выраженная дилатация левых отделов сердца с признаками ремоделирования полости ЛЖ (рис. 4).
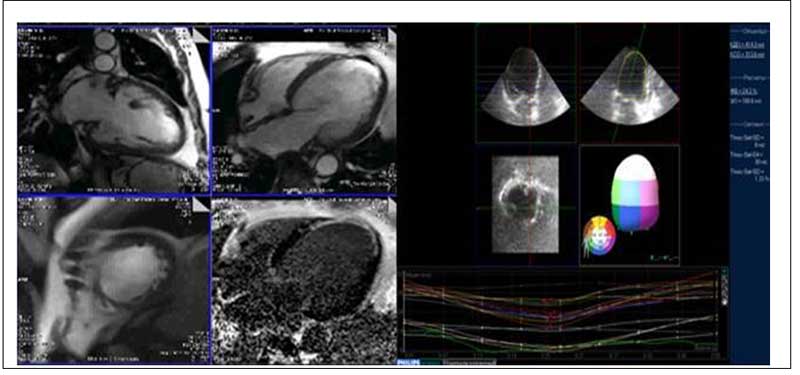
Рис. 4. Постинфарктное ремоделирование левого желудочка, оценка методами МТР и 3DЭХОКГ
Анализ линейной регрессии показал достоверную согласованность между объемными показателями и ФВЛЖ при исследовании с помоцью трехмерного УЗИ и МРТ: конечный диастолический объем (КДО) ЛЖ (медиана, М) составлял 287 мл (3DТТЭхоКГ) и 275 мл (МРТ), р>0,05, соответственно; конечный систолический объем (КСО) ЛЖ - 195 мл (3DТТЭхоКГ) и 190 мл (МРТ), р>0,05, соответственно; ФВ ЛЖ - 33 % (3DТТЭхоКГ) и 31 % (МРТ), р>0,05, соответственно.
| Параметры | 3DTTЭхоКГ | МРТ | Коэффициент ранговой корреляции Спирмена | Достоверность различий (p) критерий Манна - Уитни Uэмп (p) |
|---|---|---|---|---|
| КДО, мл | 287 206-387 178-390 |
275 198-376 170-392 | 0,72 | (>0,05) |
| КСО, мл | 195 119-208 106-224 |
190 108-216 101-240 | 0,88 | (>0,05) |
| УВ, мл | 62 31-126 30-139 |
54 32-107 32-130 | 0,80 | (>0,05) |
| ФВ, % | 33 19-42 17-46 |
31 19-44 18-46 | 0,81 | (>0,05) |
| TAPSE, мм | 15 11-19 6-22 |
|||
| FAC, % | 34 25-42 19-50 |
Примечание. На первой строке ячейки представлена медиана (50-й процентиль), на второй строке - 2,5-97,5-й процентили, на третьей строке - минимальное - максимальное значения.
Систолическая функция правого желудочка (ПЖ) полученная методами двухмерной эхокардиографии с тенденцией к снижению у всех пациентов: систолическая экскурсия плоскости трикуспидального кольца (TAPSE) - 15 мм; фракционное изменение площади ПЖ (FAC) - 34 % (таблица).
У обследованых имела место умеренная и выраженная регургитация на митральном и трикуспидальном клапанах, при этом аортальная регургитация отсутствовала или была незначительная.
Оперативные вмешательства были выполнены 3 пациентам с наибольшей степенью выраженности ремоделирования полости левого желудочка, имевших КДО более 350 мл, ФВ ЛЖ менее 20 %, гемодинамически значимое поражение церебральных сосудов и сосудов бассейнов нижних конечностей, сопутствующую реноваскулярную патологию. В связи с высоким риском интраоперационных осложнений и остановки кровообращения на этапе отключения аппарата ИК при проведении оперативного вмешательства в объеме АКШ, МКШ, эндовентрикулопластики ЛЖ с одномоментным протезированием и/или пластикой атрио-вентрикулярных (АВ) клапанов у данных больных было решено использовать транскатетерный микроаксиальный насос Impella RSS ®LP 5.0.
Применение интраоперационного ЧПЭхоКГ 2 пациентам на этапе имплантации и работы устройства помогло осуществить корректное позиционирование системы в полости ЛЖ на завершающем этапе операций, получить оптимальный позиционный сигнал, соответствующий расчетному объему крови до 4,6 л/мин. и достаточный по амплитуде пульсовой кровоток. Применение Impella RSS ®LP 5.0 на этапе остановки АИК позволило максимально сократить время искусственного кровообращения и уменьшить время окклюзии аорты.
В обоих клинических случаях за время работы девайса от 58 до 65 мин. произведены остановка ИК, подключение временной ЭКС, выполнена реперфузия миокарда с плавным снижением объемного потока. Затем на фоне полного восстановления функции миокарда остановлена и извлечена система Impella RSS ®LP 5.0.
Динамика объемных показателей, систолической функции левого и правого желудочков при ТЕЕ, полученных в режиме двухмерной биплановой эхокардиографии по алгоритму Симпсона (2DBP), претерпела закономерные изменения. К моменту подключения Impella RSS ®LP 5.0 после пластики аневризмы верхушки ЛЖ отмечалось достоверное снижение КДО ЛЖ (мл), КСО ЛЖ (мл) до 30 % по сравнению с начальным этапом операции, при этом УО ЛЖ (мл) и ФВ ЛЖ (%) значимо не изменились. Значения параметров, характеризующих систолическую функцию ПЖ (TAPSE) и (FAC) также остались прежними.
Применение девайса на фоне малого сердечного выброса и низкой ФВ ЛЖ способствовало увеличению УО ЛЖ (мл), КСО ЛЖ (мл) и ФВ ЛЖ (%) на 40 % и более, отмечалось увеличение значения показателей TAPSЕ и FAC, уменьшение степени митральной и трикуспидальной регургитации.
За время работы системы обхода ЛЖ признаков дислокации девайса и изменения позиционного сигнала не выявлено, расчетный объем крови оставался стабильным, что позволило произвести остановку ИК. На завершающем этапе операции после извлечения Impella RSS ®LP 5.0 наблюдалось закономерное снижение УО ЛЖ (мл) и ФВ ЛЖ (%). В раннем послеоперационном периоде отмечено увеличение УО ЛЖ (мл) и ФВ ЛЖ (%) до 15-20 % от исходных значений, что было подтверждено методами (2DBP, ЗDTTЭХОКГ) и МРТ.
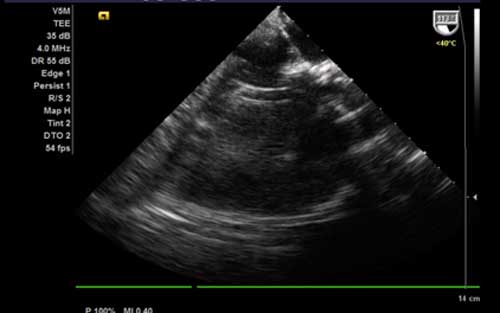
Рис. 5. Контакт камеры всасывания проксимального конца канюли Impella RSS ®LP 5.0 с боковой стенкой левого желудоч
В одном случае объективные трудности, возникшие у хирургической бригады при имплантации девайса, в связи малым КДО и невозможностью получить адекватный позиционный сигнал потребовали прекращения работы системы, что было своевременно выявлено при интраоперационном ТЕЕ. Причиной явился контакт камеры всасывания девайса с боковой стенкой ЛЖ и стойкое присасывание канюли насоса к внутрисердечныи структурам (рис. 5).
Таким образом, ЧПЭхоКГ используется перед имплантацией транскатетерного микроаксиального насоса Impella RSS ®LP 5.0 для оценки анатомических особенностей аорты и выходного тракта ЛЖ. Во время и после имплантации с помощью ТЕЕ проводится коррекция положения системы, оценивается динамика показателей систолической функции левого и правого желудочков. Необходимость совершенствования навыков УЗ контроля и расширение методов визуализации при использовании Impella RSS ®LP 5.0 играет важную роль для достижения максимальной производительности системы и уменьшения интраоперационных осложнений.
Литература |
 |
 1. Иткин Г.П. Механическая поддержка кровообращения: проблемы, решения и новые технологии// Вестник трансплантологии и искусственных органов том XVI., № 3. - 2014. doi: 10.15825/1995-1191-2014-3-76-84.
1. Иткин Г.П. Механическая поддержка кровообращения: проблемы, решения и новые технологии// Вестник трансплантологии и искусственных органов том XVI., № 3. - 2014. doi: 10.15825/1995-1191-2014-3-76-84. 2. Чернявский А.М., Доронин Д.В., Корнилов И.А., Дерягин М.Н., Фомичев А.В., Караськов А.М. Механическая поддержка у больных с терминальной сердечной недостаточностью // Клин. и эксперимент. хир. журн. им. акад. Б.В. Петровского. - 2014. - № 2. - С. 25-34.
2. Чернявский А.М., Доронин Д.В., Корнилов И.А., Дерягин М.Н., Фомичев А.В., Караськов А.М. Механическая поддержка у больных с терминальной сердечной недостаточностью // Клин. и эксперимент. хир. журн. им. акад. Б.В. Петровского. - 2014. - № 2. - С. 25-34. 3. Catena E., Milazzo F., Merli M., Paino R., Garatti A., Colombo T., Vitali E. Echocardiographic evaluation of patients receiving a new left ventricular assist device: the Impella recover 100 // Eur J Echocardiography. - 2004. - № 5. - Р. 430-437.
3. Catena E., Milazzo F., Merli M., Paino R., Garatti A., Colombo T., Vitali E. Echocardiographic evaluation of patients receiving a new left ventricular assist device: the Impella recover 100 // Eur J Echocardiography. - 2004. - № 5. - Р. 430-437. 4. Hauptman P.J., Body S., Fox J., Couper J.S., Loh E. Implantation of a pulsatile external left ventricular assist device: role of intraoperative transesophageal echocardiography // J Cardiothorac Vasc Anesth. - 1994. - № 8. - Р. 340-341.
4. Hauptman P.J., Body S., Fox J., Couper J.S., Loh E. Implantation of a pulsatile external left ventricular assist device: role of intraoperative transesophageal echocardiography // J Cardiothorac Vasc Anesth. - 1994. - № 8. - Р. 340-341. 5. Impella® 5.0 with the Impella® Controller. Instructions for Use & Clinical Reference Manual. - June 2012 Document No. 0046-9051 Rev. A. - http://www.accessdata.fda.gov/cdrh_docs/pdf14/H140001D.pdf.
5. Impella® 5.0 with the Impella® Controller. Instructions for Use & Clinical Reference Manual. - June 2012 Document No. 0046-9051 Rev. A. - http://www.accessdata.fda.gov/cdrh_docs/pdf14/H140001D.pdf. 6. Palmen M. The Impella system as a 'bridge to recovery': a case series of four ST-elevation myocardial infarction patients presenting in cardiogenic shock // Netherlands Journal of Critical Care. - 2011. -№ 8. - Р. 267.
6. Palmen M. The Impella system as a 'bridge to recovery': a case series of four ST-elevation myocardial infarction patients presenting in cardiogenic shock // Netherlands Journal of Critical Care. - 2011. -№ 8. - Р. 267. 7. Pennington D.G. Mechanical circulation support for acute heart failure // The Annals of Thoracic Surgery. - 2001. - № 71. - Р. 59.
7. Pennington D.G. Mechanical circulation support for acute heart failure // The Annals of Thoracic Surgery. - 2001. - № 71. - Р. 59.  8. Pepino P., Germano С., Piermario О., et al. Successful use of the Impella Recover LP 5.0 device for circulatorysupport during off-pump coronary artery bypass grafting // International Journal of Surgery. - 2014; Case Reports 5. - Р. 803-805.
8. Pepino P., Germano С., Piermario О., et al. Successful use of the Impella Recover LP 5.0 device for circulatorysupport during off-pump coronary artery bypass grafting // International Journal of Surgery. - 2014; Case Reports 5. - Р. 803-805. 9. Scalia G.M., McCarthy P.M., Savage R.M., Smedira N.G., Thomas J.D. Clinical utility of echocardiography in the management of implantable ventricular assist devices // J Am Soc Echocardiogr. - 2000. - № 13. - Р. 754-763.
9. Scalia G.M., McCarthy P.M., Savage R.M., Smedira N.G., Thomas J.D. Clinical utility of echocardiography in the management of implantable ventricular assist devices // J Am Soc Echocardiogr. - 2000. - № 13. - Р. 754-763. 10. Siegenthaler M.P., Brehm K., Strecker T., Hanke T., Notzold A., Olschewski M., et al The Impella recover microaxial left ventricular assist device reduces mortality for postcardiotomy failure: a three-center experience // J Thorac Cardiovasc Surg. - 2004. - № 127. - Р. 812-22.
10. Siegenthaler M.P., Brehm K., Strecker T., Hanke T., Notzold A., Olschewski M., et al The Impella recover microaxial left ventricular assist device reduces mortality for postcardiotomy failure: a three-center experience // J Thorac Cardiovasc Surg. - 2004. - № 127. - Р. 812-22. 11. Spencer F.C., Eiseman B., Trinkle J.K. Assisted circulation for cardiac failure following intra-cardiac surgery with cardiopulmonary bypass // J Thorac Cardiovasc Surg. - 1965. - № 49. - Р. 56-73.
11. Spencer F.C., Eiseman B., Trinkle J.K. Assisted circulation for cardiac failure following intra-cardiac surgery with cardiopulmonary bypass // J Thorac Cardiovasc Surg. - 1965. - № 49. - Р. 56-73. 12. Syed A.L., Kakkar A., et al. Prophylactic use of intra-aortic balloon pump for high-risk percutaneous coronary intervention: will the Impella LP 2.5 device show superiority in a clinical randomized study? // Cardiovasc. Revasc. Med. - 2011. - № 12. - Р. 72.
12. Syed A.L., Kakkar A., et al. Prophylactic use of intra-aortic balloon pump for high-risk percutaneous coronary intervention: will the Impella LP 2.5 device show superiority in a clinical randomized study? // Cardiovasc. Revasc. Med. - 2011. - № 12. - Р. 72.
 |
Главное меню |
 |
Заглавие |
 |
Введение |
 |
Материалы и методы |
 |
Результаты и обсуждение |
 |
Литература |
Оригинальная верстка  |
|
Телефон: (4212) 76-13-96
«Дальневосточный медицинский журнал»