2019 год № 2
Внутренние болезни
2 301 Военный клинический госпиталь МО РФ, 680000, ул. Серышева, 1, тел. 8-(4212)-39-47-82;
3Консультативно-диагностический центр "Вивея", 680000, ул. Запарина, 83, тел. 8-(4212)-45-15-40, г. Хабаровск
Резюме:
Ключевые слова:
2Military Hospital № 301, Defense Ministry of the Russian Federation;
3The Consultative Diagnostic Center "Vivea", Khabarovsk
Summary:
Key words:
Введение |
 |
 |
В настоящее время в мире в целом и в России в частности одним из самых распространенных сердечно-сосудистых заболеваний, а также главнейшим фактором риска развития инсульта и инфаркта миокарда остается артериальная гипертензия (АГ) [13]. Поданным исследования ЭССЕ РФ частота АГ в нашей стране составляет около 43 % среди трудоспособного населения [3]. Отрицательная роль повышенного артериального давления (АД) как триггера сердечно-сосудистого континуума значимо возрастает, если оно одновременно сочетается с другими факторами риска (ФР), в первую очередь курением, ожирением, нарушением липидного и углеводного обменов [13]. Последние три из перечисленных ФР включены в такое понятие, как метаболический синдром (МС). Основными патогенетическими составляющими данного синдрома считают наличие инсулинорезистентности и активации ренин-ангиотензин-альдостероновой системы (РААС) [5]. Поэтому, при выборе антигипертензивной терапии (АГТ) у данной категории пациентов предпочтение отдается препаратам, блокирующим РААС - ингибиторам ангиотензинпревращающего фермента (ИАПФ) или блокаторам рецепторов ангиотензина 1 типа (БРА) [13], у каждого из которых есть свои особенности и дополнительные свойства [2, 5].
Цель работы состояла в оценке влияния Телмисартана (Танидол®, "Гедеон Рихтер") на динамику офисного и суточного АД, состояние сосудистой жесткости и метаболические ФР у пациентов среднего возраста с АГ и МС.
Материалы и методы
|
 |
 |
Оригинальное проспективное открытое наблюдательное исследование. Первоначально были включены 47 пациентов с АГ и МС, одна больная выбыла через 2 недели, окончательно включено в анализ 46 больных, средний возраст - 54,7±1,4 лет, мужчин/женщин - 34 (73,9 %) /12 (26,1 %). Диагноз АГ устанавливался на основании Рекомендаций ESH/ESC 2013 года [10], МС - по Российским рекомендациям 2010 года [5]. Критерии включения: мужчины и женщины в возрасте 45-65 лет с АГ 1-2-й степени в сочетании с МС, исходно нелеченые или леченые неэффективно в предшествующие 6 месяцев, отсутствие критериев исключения. Критерии исключения: возраст старше 65 лет, симптоматическая АГ, гипертензия третьей степени или АД выше 170/100 мм рт. ст., при которой необходим прием 3 и более антигипертензивных препаратов, инфаркт миокарда, нестабильная стенокардия или нарушение мозгового кровообращения в течение 3 месяцев до начала участия в исследовании, фибрилляция предсердий, хроническая сердечная недостаточность III-IV ФК по NYHA, тяжелые сопутствующие заболевания и состояния (по мнению лечащего врача), злоупотребление алкоголем, значительные нарушения функции почек (клиренс креатинина 30 мл/мин. и ниже), печени (активность аминотрансфераз выше верхней границы нормы в 2 раза); злокачественные новообразования; гиперчувствительность к телмисартану, или любому из компонентов в составе таблетки АГ; отказ пациента от начала и продолжения исследования. Работа одобрена локальным этическим комитетом при ФГБОУ ВО "ДВГМУ" Минздрава России в соответствии с положением Хельсинской декларации по вопросам медицинской этики и на основании ст. 43 "Основ законодательства Российской Федерации об охране здоровья граждан" в редакции законов от 02.03.1998 г. № 30-ФЗ, от 20.12.1999 г. № 214-ФЗ соответствует общепринятым нормам морали, требованию соблюдения прав, интересов и личного достоинства лиц, принимавших участие в исследовании и не представляет риска для участников. Набор и наблюдение за пациентами происходили с января по октябрь 2017 года в двух амбулаторно-поликлинических учреждениях г. Хабаровска. Подробная характеристика всей группы пациентов, включенных в исследование, представлена в таблице 1.
Дизайн исследования предусматривал 4 визита больного к врачу: первый (Н0) - визит включения, где приводилась оценка исследуемых параметров, отменялась предшествующая АГТ и назначался телмисартан в виде моно или комбинированной терапии в дозах и сочетаниях с другими антигипертензивными препаратами (АГП) по усмотрению врача, это же касалось и другой необходимой терапии. Второй (Н2), третий (Н4) и четвертый (Н12) - контрольные визиты через 2, 4 и 12 недель соответственно. На Н2 визите проводили, если требовалось, коррекцию лечения, на Н12 - повторное полное обследование. Перед включением в исследование ИАПФ/БРА, кроме телмисартана принимали 69,5 %, диуретики, преимущественно индапамид - 30,4 %, бета-блокаторы - 26,1 %, амлодипин - 28,3 %, статины - 30,4 % (аторвастатин 20 мг/сут. или розувастатин 10-20 мг/сут.), аспирин - 8,7 %, пероральные сахароснижающие препараты - 39,1 % (метформин 850-1 000 мг дважды в день, вилдаглиптин 50 мг/сут., гликлазид 60 мг/сут. и различные типы инсулинов - 4,3 пациентов (хумулин 20/10 ЕД/сут. и инсулин гларгин 60 Ед/сут.). Перечисленные дозы препаратов не изменялись в течение периода исследования.
Всем больным проводили офисное измерение АД согласно требуемым правилам [10]. Суточное мониторирование АД (СМАД) осуществляли с помощью автоматической амбулаторной системы суточного мониторирования BPLab МнСДП-2 (ООО "Петр Телегин"). Оценку состояния артериальной ригидности проводили методом объемной сфигмографии на аппарате "VaSera-1000" ("Fukuda Denshi", Япония). Определяли скорость распространения пульсовой волны (СРПВ, м/сек), сердечно-лодыжечный сосудистый индекс (CAVI), лодыжечно-плечевой индекс (ЛПИ) и индекс аугментации (AIX). Оценивали показатели липидного спектра, содержание креатинина крови с расчётом его клиренса по CKD-EPI в мл/мин./1,73, мочевой кислоты и содержание аминотрансфераз. Уровень глюкозы определяли гексокиназным методом (на автоматическом анализаторе La Roche). Инсулин плазмы - иммуноферментным способом (Insulin ELISA (Mercodia AB, Швеция), уровень гликозилированного гемоглобина (HbАC1 в %) на анализаторе DS-5 Glycomat. Индекс инсулинорезистентности HOMA-IR рассчитывали по формуле: глюкоза натощак (ммоль/л) × инсулин натощак (мкЕд/мл)/22,5. Определяли индивидуальный сердечно-сосудистый риск по шкале SCORE. Сравнительный анализ частоты распределения оцениваемых показателей и равенства дисперсий изучаемых признаков проводился с помощью пакетов статистических программ Statistica 6.0. Нормальность распределения оценивали при помощи критерия Колмогорова - Смирнова. Использовали вычисление средних величин и стандартных ошибок. Определение связи между изучаемыми величинами - методом корреляционного анализа по Спирмену. Равенство дисперсий при наличии ненормального распределения, а также малое число совпадений в сравниваемых группах значений признака определило в качестве основного критерия U-критерий Манна - Уитни и точного критерия Фишера. Критический уровень значимости при проверке статистических гипотез принимался р<0,05.
| Показатель | Величина |
|---|---|
| Всего обследованных пациентов | 46 |
| Средний возраст (лет) | 54,7±1,4 |
| Мужчин/женщин n (%) | 34(73,9 %)/12 (26,1 %) |
| Средняя длительность АГ (лет) | 10,2±1,2 |
| АГ 1-й степени n (%) | 28 (60,9) |
| АГ 2-й степени n (%) | 18 (39,1) |
| ИМТ (кг/м2) | 31,2±0,64 |
| ОТ, (см) вся группа | 102,9±1,9 |
| ОТ мужчины (см) | 107,1±2,4 |
| ОТ женщины (см) | 91,8±2,2 |
| ОХС (ммоль/л) | 5,68±0,14 |
| ЛПНП (ммоль/л) | 3,5±0,14 |
| ЛПВП (ммоль/л) | 1,32±0,6 |
| ТГ (ммоль/л) | 1,9±0,14 |
| Курение n (%) | 5 (10,9) |
| Сахарный диабет/НТГ n (%) | 13 (28,3)/7 (15,2) |
| ЦВЗ: ОНМК (в анамнезе) n (%) | 2 (4,3) |
| ИБС: стенокардия, ИМ (в анамнез) n (%) | 3 (6,5) |
Примечание. ОТ - объем талии, НТГ - нарушение толерантности к глюкозе, ЦВЗ - цереброваскулярное заболевание, ОНМК - острое нарушение мозгового кровообращения, ИМ - инфаркт миокарда.
Результаты и обсуждение
|
 |
 |
На протяжении указанного периода наблюдения дозу телмисартана 40 мг/сут принимали 26 (56,5 %) и 80 мг/сут. (43,5 %) пациентов, среднесуточная доза препарата составила 57,4±5,8 мг. При этом телмисартан в качестве монотерапии был у 13 (29,3 %) пациентов, остальные 33 (71,7 %) получали комбинированную АГТ. Из них 27 (58,7%) больных - двойную комбинацию, чаще всего с индапамидом 1,5 мг/сут. (16 - 34,8 %), реже с амлодипином 5-10 мг/сут. (7 - 15,2 %) и бисопрололом 5-10 мг/сут. (4 - 8,7 %). 6-ти пациентам (13 %) потребовалось тройная терапия (телмисартан, индапамид и амлодипин).
Исходно (Н0) среднее значение офисного систолического АД (САД) составило 152,3±2,6 мм рт. ст. При втором визите (Н2) отмечали снижение САД до 139,2±1,9 мм рт. ст., р=0,002, которое продолжало снижаться и к Н4 достигло 127,7±1,2 мм рт. ст., р=0,001. За двенадцать недель терапии среднее снижение офисного САД составило 23,7±1,9 мм рт. ст. Офисное диастолическое АД (ДАД) первоначально (Н0) было 91,3±1,6 мм рт. ст. На визите Н2 также наблюдали его достоверное снижение (86,6±1,6 мм рт. ст., р=0,039) и к Н12 оно достигло 79,8±0,9 мм рт. ст., р=0,001. В среднем снижение офисного ДАД было 11,8±1,4 мм рт. ст. (табл. 2). Аналогичная динамика была отмечена при оценке параметров СМАД. САДд за период Н0-Н12 составило 144,6±1,8 и 135,1±1,9 мм рт. ст., р=0,001; САДн - 130,4±2,4 и 118,6±2,5 мм рт. ст., р=0,001; ДАДд - 89,2±1,4 и 82,2±1,2 мм рт. ст., р=0,001; ДАДн - 76,4±1,3 и 72,5±1,6 мм рт. ст., р=0,065 соответственно (табл. 3). При оценке СМАД наблюдали изменения и со стороны суточных профилей АД. Увеличился процент пациентов с профилем "диппер" по САД с 41,3 % до 60,9 %, р=0,007, по ДАД - с 39,1 % до 56,4 %, р=0,023 и уменьшился - с профилем "найт-пикер" по САД с 19,6 % до 0,0 %, р=0,001 и по ДАД с 13,3 % до 2,3 %, р=0,002 (рис. 1, 2).
Через двенадцать недель (Н12) от начала терапии телмисартаном наблюдали значимое снижение СРПВ по отношению к Н0 (8,36±0,36 и 6,79±0,32 м/сек, р=0,002), остальные параметры артериальной ригидности не претерпевали изменений (табл. 4).
| АД | Н0 | Н2 | Н4 | Н12 |
|---|---|---|---|---|
| САД | 152,3±2,6 р=0,002 р1=0,001 | 139,2±1,9 р3=0,018 р4=0,001 | 133,2±1,6 р5=0,008 | 127,7±1,2 р2=0,001 |
| Среднее снижение САД | 23,7±1,9 | |||
| ДАД | 91,3±1,6 р=0,039 р1=0,001 | 86,6±1,6 р3=0,073 р4=0,001 | 82,9±1,3 р5=0,05 | 79,8±0,9 р2=0,001 |
| Среднее снижение ДАД | 11,8±1,4 | |||
Примечание. р - Н0-Н2; р1 - Н0-Н4; р2 - Н0-Н12; р3 - Н2-Н4; р4 - Н2-Н12; р5 - Н4-Н2; Н0 - исходно; Н2 - через 2 недели; Н4 - через 4 недели; Н12 - через 12 недель.
| АД | Н0 | Н12 | Разница |
|---|---|---|---|
| САДд | 144,6±1,8 | 135,1±1,9, р=0,001 | 10,6±1,8 |
| САДн | 130,4±2,4 | 118,6±2,5, р=0,001 | 12,4±2,1 |
| ДАДд | 89,2±1,4 | 82,2±1,2, р=0,001 | 7,3±1,1 |
| ДАДн | 76,4±1,3 | 72,5±1,6, р=0,065 | 4,5±1,3 |
Примечание. р - Н0-Н12.
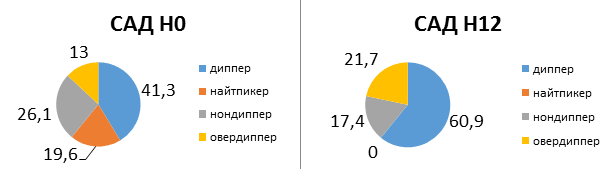
Рис. 1. Типы суточного профиля САД по данным СМАД (в %) исходно и через 12 недель
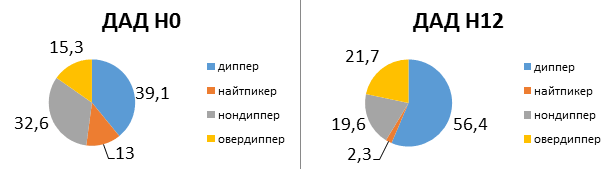
Рис. 2. Типы суточного профиля ДАД по данным СМАД (в %) исходно и через 12 недель
Через 12 недель от начала лечения не было установлено, каких-либо изменений со стороны метаболических факторов риска по отношению к первоначальным значениям, а также негативного влияния на функцию почек и печени (табл. 5).
| Показатель | Н0 | Н12 | р |
|---|---|---|---|
| СРПВ (м/с) | 8,36±0,36 | 6,79±0,32 | 0,002 |
| ЛПИ справа | 1,07±0,02 | 1,32±0,2 | 0,245 |
| ЛПИ слева | 1,07±0,2 | 1,05±0,02 | 0,724 |
| CAVI справа | 7,73±0,2 | 7,49±0,2 | 0,41 |
| CAVI слева | 7,91±0,18 | 7,63±0,17 | 0,256 |
| AIX | 1,19±0,07 | 1,4±0,23 | 0,4 |
| Показатель | Н0 | Н12 | р |
|---|---|---|---|
| ИМТ (кг/м2) | 31,2±0,64 | 30,9±0,62 | 0,79 |
| ОТ, все (см) | 102,9±1,9 | 101,9±1,9 | 0,73 |
| ОТ мужчины (см) | 107,1±2,4 | 106,2±2,9 | 0,64 |
| ОТ женщины | 91,8±2,2 | 91,0±3,1 | 0,71 |
| ОХС (ммоль/л) | 5,68±0,14 | 5,27±0,15 | 0,05 |
| ЛПНП (ммоль/л) | 3,5±0,14 | 3,14±0,14 | 0,058 |
| ЛПВП (ммоль/л) | 1,32±0,6 | 1,37±0,6 | 0,56 |
| ТГ (ммоль/л) | 1,9±0,14 | 1,74± | 0,41 |
| Глюкоза (ммоль/л) | 6,41±0,23 | 6,28±0,14 | 0,631 |
| Инсулин (мкЕд/мл) | 12,81±1,3 | 11,8±1,2 | 0,657 |
| HOMA-IR | 3,85±0,22 | 3,67±0,28 | 0,594 |
| HbАC1 (%) | 5,45±0,1 | 5,72±0,11 | 0,068 |
| Мочевая кислота (ммоль/л) | 0,336±0,1 | 0,334±0,1 | 0,958 |
| Креатинин (ммоль/л) | 0,157±0,04 | 0,155±0,04 | 0,842 |
| СКФ (CKD-EPI) мл/мин/1,73 | 79,6±1,7 | 84,0±2,2 | 0,114 |
| АЛАТ (Е/л) | 29,2±1,8 | 27,8±1,3 | 0,532 |
| АСАТ (Е/л) | 28,7±1,4 | 26,9±1,1 | 0,343 |
Оценка общего сердечно-сосудистого риска по шкале SCORE показала, что он снизился с 5,89±0,51 до 3,6±0,36, р=0,001.
Согласно последним европейским рекомендациям по диагностике и лечению АГ 2018 года, средства, блокирующие РААС (ИАПФ и БРА), являются приоритетными при лечении как неосложненной АГ, так и при ее сочетании с другой кардиальной или почечной патологией, а также сахарным диабетом (СД) и МС. При этом практические отсутствуют особые преференции при выборе каждого из классов АГП [13]. Последнее обусловлено тем, что при непосредственном сравнении ИАПФ и БРА продемонстрировали аналогичные влияния на сердечно-сосудистые исходы и общую смертность у пациентов с АГ [1, 11, 12]. В этой связи, рабочая группа по АГ Российского кардиологического общества пришла к заключению, что "…сартаны являются одним из наиболее эффективных и безопасных классов АГП среди рекомендуемых для терапии пациентов с АГ, снижающих риск развития сердечно-сосудистых, цереброваскулярных и почечных осложнений" Тем не менее, для каждого конкретного препарата из группы БРА существуют свой специфический выбор, основанный на доказательной базе [2].
В настоящее время в большом числе работ показано, что важную роль в процессах атерогенеза играют PPAR-γ рецепторы, при этом их недостаточная активность способствует прогрессированию атеросклероза. Поэтому препараты, способные повышать активность указанных рецепторов, могут существенно снижать инсулинорезистентность, уровень триглицеридов и, соответственно, риск развития атеросклероза. Доказано, что именно телмисартан, в дополнение к блокаде АТ1 рецептора, способен частично активировать PPAR-γ-рецепторы [4, 7]. Именно двойной механизм действия телмисартана продемонстрировал его способность обеспечивать защиту от атеросклероза и коронарных событий и снижать риск возникновения СД пациентов с высоким сердечно-сосудистых риском [8, 9]. Благодаря указанным механизмам действия: селективной блокаде АТ1-рецепторов и частичной активации PPAR-γ рецепторов телмисартан рекомендован к качестве препарата выбора из класса сартанов для лечения больных с МС [2].
Другой важной проблемой у пациентов с МС и СД является повышенная артериальная жесткость, которая с большой частотой встречается среди данной категории пациентов. Хроническая гипергликемия и гиперинсулинемия увеличивают активность локальной РААС, экспрессию рецепторов ангиотензина 1-го типа в сосудистой стенке с последующим развитием фиброза [6]. В этой связи, способность АГП уменьшать артериальную ригидность является важным дополнительным критерием при его назначении. Телмисартан в ряде исследований продемонстрировал свою способность снижать артериальную жесткость у пациентов с АГ [4].
Необходимо подчеркнуть, что все представленные положительные свойства телмисартана были получены на оригинальном препарате. В настоящее время отечественный рынок лекарственных средств представлен рядом дженериков телмисартана, отвечающим стандартам GMP (Good Manufacturing Practic, Надлежащая производственная практика), среди которых присутствует и Танидол®, ОАО "Гедеон Рихтер". Результаты проведенного исследования показали, что данный телмисартан обладает высокой антигипертензивной эффективностью, как в отношении офисного АД, так и при проведении СМАД. Достигнутые целевые значения офисного АД менее 130/80 мм рт. ст. соответствуют современным критериям АГТ [13]. При этом 12-недельная терапия способствовала увеличению процента пациентов физиологически суточным профилем АД "диппер" и снижению с профилем "найт-пикер", что важно с позиций защиты органов-мишеней. Подтверждением тому служит способность препарата снижать СРПВ у данной категории пациентов. Учитывая небольшую длительность наблюдения, в первую очередь за счет снижения САД, как офисного, так и при оценке СМАД, что подтверждалось и результатами корреляционного анализа (офисное САДН12/СРПВ r=0,3016, p<0,05; САДдН12/СРПВ r=0,3574, p<0,05; САДнН12/СРПВ r=0,4131, p<0,05). Мы не выявили влияние данного препарата на метаболические ФР, что с одной стороны свидетельствовало о его безопасности и хорошей переносимости, с другой - для получения положительных результатов, по видимому, требуется более длительный срок наблюдения.
Данная работа, безусловно, имеет определенные ограничения в первую очередь из-за малого количества включенных в нее пациентов и небольшого периода наблюдения. Вместе с тем полученные результаты представляют несомненный интерес и требуют дальнейших исследований.
Авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье. Препарат Танидол® для исследования был предоставлен ОАО "Гедеон Рихтер".
Выводы
|
 |
 |
1. У пациентов среднего возраста с АГ и МС телмисартан (Танидол®, ОАО "Гедеон Рихтер") эффективно контролирует офисное и суточное АД.
2. Препарат способствует увеличению числа пациентов с физиологическим суточным профилем АД.
3. 12-недельная терапия данным АГП приводила к достоверному снижению скорости распространения пульсовой волны.
Литература |
 |
 1. Гямджян К.А., Максимов М.Л. Сартаны и ингибиторы ангиотензинпревращающего фермента поединок двух лидеров в фармакотерапии сердечно-сосудистых заболеваний // РФК. - 2012. - № 8 (6). - С. 826-830.
1. Гямджян К.А., Максимов М.Л. Сартаны и ингибиторы ангиотензинпревращающего фермента поединок двух лидеров в фармакотерапии сердечно-сосудистых заболеваний // РФК. - 2012. - № 8 (6). - С. 826-830. 2. Конради А.О., Жданова О.Н., Ротарь О.П и др. Заключение рабочей группы по артериальной гипертонии. Место сартанов в терапии артериальной гипертонии в XXI веке // Российский кардиологический журнал. - 2018. - № 3 (155). - С. 76-81.
2. Конради А.О., Жданова О.Н., Ротарь О.П и др. Заключение рабочей группы по артериальной гипертонии. Место сартанов в терапии артериальной гипертонии в XXI веке // Российский кардиологический журнал. - 2018. - № 3 (155). - С. 76-81. 3. Муромцева Г.А., Концевая А.В., Константинов В.В и др. Распространённость факторов риска неинфекционных заболеваний в Российской популяции в 2012-2013 гг. Результаты исследования ЭССЕ-РФ // Кардиоваскулярная терапия и профилактика. - 2014. - № 13 (6). - С. 4-11.
3. Муромцева Г.А., Концевая А.В., Константинов В.В и др. Распространённость факторов риска неинфекционных заболеваний в Российской популяции в 2012-2013 гг. Результаты исследования ЭССЕ-РФ // Кардиоваскулярная терапия и профилактика. - 2014. - № 13 (6). - С. 4-11. 4. Остроумова О.Д., Кочетков А.И., Смолярчук Е.А. и др. Возможности телмисартана в снижении сердечно-сосудистого риска // Кардиоваскулярная терапия и профилактика. - 2018. - № 17 (1). - С. 87-96.
4. Остроумова О.Д., Кочетков А.И., Смолярчук Е.А. и др. Возможности телмисартана в снижении сердечно-сосудистого риска // Кардиоваскулярная терапия и профилактика. - 2018. - № 17 (1). - С. 87-96. 5. Рекомендации экспертов Всероссийского научного общества кардиологов по диагностике и лечению метаболического синдрома. Второй пересмотр // Практическая медицина. - 2010. - № 5 (44). - С. 81-101.
5. Рекомендации экспертов Всероссийского научного общества кардиологов по диагностике и лечению метаболического синдрома. Второй пересмотр // Практическая медицина. - 2010. - № 5 (44). - С. 81-101. 6. Adel M., ELSheikh A., Sameer S., et al. Arterial stiffness in metabolic syndrome // J Saudi Heart Assoc. - 2016. - Vol. 28. - P. 249-256.
6. Adel M., ELSheikh A., Sameer S., et al. Arterial stiffness in metabolic syndrome // J Saudi Heart Assoc. - 2016. - Vol. 28. - P. 249-256. 7. Jugdutt BI. Clinical effectiveness of telmisartan alone or in combination therapy for controlling blood pressure and vascular risk in the elderly // Clin Interv Aging. - 2010. - Vol. 5. - P. 403-416.
7. Jugdutt BI. Clinical effectiveness of telmisartan alone or in combination therapy for controlling blood pressure and vascular risk in the elderly // Clin Interv Aging. - 2010. - Vol. 5. - P. 403-416. 8. Kakuta H., Sudoh K., Sasamata M., Yamagishi S. Telmisartan has the strongest binding affinity to angiotensin II type 1 receptor: comparison with other angiotensin II type 1 receptor blockers // Int J Clin Pharmacol Res. - 2005. - Vol. 25 (1). - P. 41-46.
8. Kakuta H., Sudoh K., Sasamata M., Yamagishi S. Telmisartan has the strongest binding affinity to angiotensin II type 1 receptor: comparison with other angiotensin II type 1 receptor blockers // Int J Clin Pharmacol Res. - 2005. - Vol. 25 (1). - P. 41-46. 9. Kurtz Th. W. New Treatment Strategies for Patients with Hypertension and Insulin Resistance // The American Journal of Medicine. - 2006. - Vol. 119 (5A). - P. 24S-30S.
9. Kurtz Th. W. New Treatment Strategies for Patients with Hypertension and Insulin Resistance // The American Journal of Medicine. - 2006. - Vol. 119 (5A). - P. 24S-30S. 10. Mancia G., Fagard R., Narkiewicz K., et al. Guidelines for the Management of Arterial hypertension: The Task Force for the Management of Arterial hypertension of the European society of hypertension (ESH) and of the European society of Cardiology (ESC) (2013) // J. hypertens. - 2013. - № 31 (7). - Р. 1281-1357.
10. Mancia G., Fagard R., Narkiewicz K., et al. Guidelines for the Management of Arterial hypertension: The Task Force for the Management of Arterial hypertension of the European society of hypertension (ESH) and of the European society of Cardiology (ESC) (2013) // J. hypertens. - 2013. - № 31 (7). - Р. 1281-1357. 11. Otto C.M. Heartbeat: Renin-angiotensin system blockade for prevention of cardiovascular disease // Heart. - 2017. - Vol. 103. - P. 1305-1307.
11. Otto C.M. Heartbeat: Renin-angiotensin system blockade for prevention of cardiovascular disease // Heart. - 2017. - Vol. 103. - P. 1305-1307. 12. Vega I.L. ACE Inhibitors vs ARBs for Primary Hypertension // Am Fam Physician. - 2015. - Vol. 91 (8). - P. 522-523.
12. Vega I.L. ACE Inhibitors vs ARBs for Primary Hypertension // Am Fam Physician. - 2015. - Vol. 91 (8). - P. 522-523. 13. Williams B., Mancia G., Spiering W., et al. 2018 ESC/ESH Guidelines for hemanagement of arterial hypertension // Eur Heart J. - 2018. - Vol. 39. - P. 3021-3104.
13. Williams B., Mancia G., Spiering W., et al. 2018 ESC/ESH Guidelines for hemanagement of arterial hypertension // Eur Heart J. - 2018. - Vol. 39. - P. 3021-3104.
 |
Главное меню |
 |
Заглавие |
 |
Введение |
 |
Материалы и методы |
 |
Результаты и обсуждение |
 |
Выводы |
 |
Литература |
Оригинальная верстка  |
|
Телефон: (4212) 76-13-96
«Дальневосточный медицинский журнал»