2021 год № 1
Клиническая медицина
2Дальневосточный государственный медицинский университет, 680000, ул. Муравьева-Амурского, 35, тел./факс 8-(4212)-30-53-11, e-mail: nauka@mail.fesmu.ru, г. Хабаровск
Резюме:
Ключевые слова:
2Far Eastern State Medical University, Khabarovsk
Abstract:
Key words:
Введение |
 |
 |
Диабетический макулярный отек является основной причиной потери зрения у пациентов c сахарным диабетом (СД). В качестве факторов риска развития диабетической ретинопатии и диабетического макулярного отека выступают неадекватный контроль гликемии, артериального давления, нарушения липидного обмена, ожирение, длительность течения СД более 10 лет, нефропатия [5, 14, 19, 28].
По данным исследования Wisconsin Epidemiological Study of Diabetic Retinopathy (WESDR) через 5 лет после начала СД 1 типа диабетическая ретинопатия выявляется у 20 % больных. С увеличением "стажа" сахарного диабета вероятность развития диабетической ретинопатии значительно возрастает, так через 10 лет она выявляется уже у 60 % пациентов, а через 20-30 лет - практически у всех пациентов с полной потерей зрения у каждого 30-го. Те же закономерности справедливы и для СД 2 типа: через 20 лет после начала заболевания 2/3 пациентов имеют диабетическую ретинопатию, причем у 20 % больных она выявляется на пролиферативной стадии [5, 19, 20].
По данным различных авторов, частота диабетического макулярного отека варьирует в зависимости от типа и длительности СД и составляет от 2,1 до 84 %. Исследования контроля СД и его осложнений показали, что диабетический макулярный отек у пациентов с СД1 в 27 % случаев развивается в течение 9 лет после начала заболевания. У пациентов с СД2 распространенность макулярного отека также возрастает с увеличением длительности диабета: с 3 % случаев при длительности заболевания менее 5 лет до 28 % при длительности 20 лет и более [2, 15].
И если при фокальном диабетическом макулярном отеке нецентральной локализации лазеркоагуляция сетчатки может быть достаточной и эффективной, то центральный или диффузный отек выступают показаниями к анти-VEGF терапии [4, 6, 23].
В настоящее время мировым стандартом лечения диабетического макулярного отека является интравитреальное введение анти-VEGF препаратов, блокирующих ключевой фактор его патогенеза - сосудистый эндотелиальный фактор роста - VEGF (vascular endothelial growth factor) [4, 9, 24, 27].
Ранибизумаб (Луцентис) представляет собой генно-инженерный гуманизированный антигенсвязывающий фрагмент антитела к VEGF, блокирующий все изоформы VEGF-A. Данные многоцентровых рандомизированных контролируемых исследований RESOLVE, RESTORE и DRCR.net показали высокую эффективность и безопасность интравитреального введения ранибизумаба для лечения диабетического макулярного отека [10, 17, 18, 21, 22, 25]. За счет уменьшения толщины сетчатки ранибизумаб позволяет стабилизировать или улучшить зрительные функции.
Показаниями к витрэктомии с пилингом внутренней пограничной мембраны (ВМП) являются пролиферативная диабетическая ретинопатия тяжёлой стадии и диабетический макулярный отек, как с тракционным компонентом, так и без него [1, 3, 11, 12]. Однако в послеоперационном периоде диабетический макулярный отек может не только сохраняться, но и прогрессировать, несмотря на положительный эффект операции.
Наши наблюдения подтвердили положительное влияние интраокулярного введения ранибизумаба на регресс диабетического макулярного отека и повышение остроты зрения в глазах после витрэктомии с пилингом ВПМ [7, 8].
Тем не менее, сравнительная оценка эффективности анти-VEGF терапии диабетического макулярного отека в глазах после витрэктомии с пилингом ВМП при различных стадиях диабетической ретинопатии с различной морфологией макулярного отека нами ранее не проводилась.
Цель работы - анализ клинической эффективности анти-VEGF терапии ДМО в авитричных глазах.
Материалы и методы
|
 |
 |
Было обследовано 38 глаз 34 пациентов с ДМО, на которых ранее проводилось эндовитреальное вмешательство по поводу ДР. Из них была сформирована основная группа. Возраст пациентов составил от 33 до 68 лет (в среднем 58±9 лет). Мужчин было 10, женщин - 24. СД 1 типа имел место у 10 пациентов (29 %), СД 2 типа - у 24 (71 %), в том числе, у 16 - вторичный инсулинозависимый. Средняя продолжительность СД составила 12,4±4,1 лет (от 5 до 20 лет). Все пациенты были не компенсированы по уровню гликемии, средний уровень сахара крови у них составлял 8,1±4,3 ммоль/л.
Использовалась одобренная ВОЗ классификация ДР по Kohner E. и Porta M. [1].
В основной группе у 18 пациентов на 18 глазах имела место тяжелая непролиферативная - препролиферативная ДР (ППДР) с диффузным ДМО с тракционным компонентом. У 14 пациентов ранее проводилась лазеркоагуляция сетчатки.
В 20 глазах 16 пациентов имела место ПДР с диффузным ДМО (рис. 1, 2). В 14 глазах 14 пациентов данной подгруппы имели место гемофтальм и глиоз диска зрительного нерва и аркад. В 4 глазах 4 пациентов ДМО имел тракционный характер. В 5 глазах 5 пациентов был выявлен рубеоз радужки.
До начала анти-VEGF терапии на всех глазах было проведено эндовитреальное вмешательство, в 14 глазах - с эндолазеркоагуляцией зон ишемии и дефектов сетчатки, завершившееся во всех случаях тампонадой силиконовым маслом, продолжавшейся в течение 2-5 месяцев. В 26 глазах через месяц после хирургии была проведена панретинальная лазеркоагуляция сетчатки.
Интравитреальное введение 0,5 мг луцентиса проводилось по стандартной схеме: три ежемесячные инъекции, далее - в режиме "по потребности". Оно было выполнено во всех 38 глазах спустя 1-2 месяца после удаления силикона. Период наблюдения составил от 6 месяцев до 6 лет.
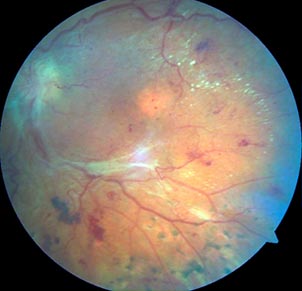
Рис. 1. Фотография глазного дна левого глаза пациентки М. Пролиферативная диабетическая ретинопатия, тракционный диабетический макулярный отек. Глиоз диска зрительного нерва и аркад, в заднем полюсе - диффузный отек, экссудация, микроаневризмы, ретроэкваториально - лазеркоагуляты, геморрагии
Группу сравнения составили 40 глаз 40 пациентов с ДМО на фоне ППДР (20 глаз - 50 %) и ПДР (20 глаз - 50 %) с нативным стекловидным телом (рис. 3, 4). Среди данных пациентов было 28 женщин (70 %) и 12 мужчин (30 %). У 38 пациентов (95 %) имел место СД 2 типа. 24 пациентам (60 %) ранее проводилась лазеркоагуляция сетчатки, 16 пациентов (40 %) ранее лечение не получали. Все пациенты группы сравнения также были не компенсированы по уровню гликемии, средний уровень сахара крови у них составлял 8,9±1,9 ммоль/л.
Пациентам группы сравнения проводилось интравитреальное введение 0,5 мг луцентиса по стандартной схеме: три ежемесячные инъекции, далее - в режиме "по потребности" до регресса ДМО. Период наблюдения также составил от 6 месяцев до 6 лет.
Всем пациентам проводилось офтальмологическое обследование с фоторегистрацией состояния глазного дна на фундус-камере Visucam 500 Carl Zeiss (Германия). Динамика ДМО оценивалась методом оптической когерентной томографии (ОКТ) на приборе Cirrus HD-OCT Model 5000 (Германия) с использованием протокола сканирования Macular Cube 512?128. Толщина сетчатки в фовеальной области исследовалась с помощью протокола Macular Thickness Analysis. Обследование проводилось до начала анти-VEGF терапии, на промежуточных этапах перед ведением луцентиса и через 1 месяц после завершения лечения.
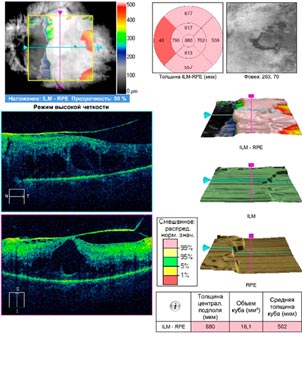
Рис. 2. Оптическая когерентная томография макулы левого глаза пациентки М. Массивная витреоретинальная тракция, кистозный макулярный отек
Статистическая обработка данных выполнялась с использованием программы IBM SPSS Statistics 20. Данные представлены в виде M±σ, где M - среднее значение, σ - стандартное отклонение. Количественные признаки сравнивались с использованием критерия U Манна-Уитни. Критический уровень значимости равен 0,05.
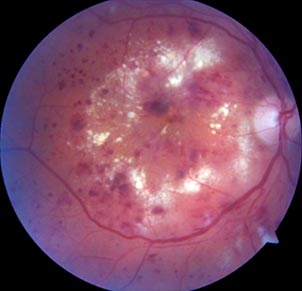
Рис. 3. Фотография глазного дна правого глаза пациента Д. Препролиферативная диабетическая ретинопатия, диабетический макулярный отек. В заднем полюсе - диффузный отек, массивная экссудация, микроаневризмы, геморрагии, ретроэкваториально - "ватообразные" очаги
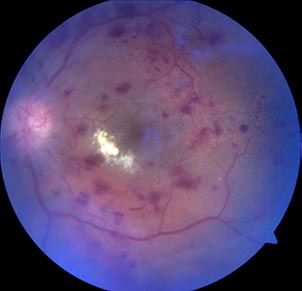
Рис. 4. Фотография глазного дна левого глаза пациента Р. Пролиферативная диабетическая ретинопатия, диабетический макулярный отек. Эпипапиллярная неоваскуляризация, в заднем полюсе диффузный отек, микроаневризмы, геморрагии, следы лазеркоагулятов, ретинальная неоваскуляризация
Результаты и обсуждение
|
 |
 |
После эндовитреального вмешательства, перед началом анти-VEGF терапии во всех 38 глазах пациентов основной группы имел место диффузный ДМО. По данным ОКТ, в 20 глазах (53 %) имела место локальная отслойка нейроэпителия (ОНЭ), в 22 глазах (58 %) отек имел кистозный характер (таблица 1; рис. 5, 6). Исходная толщина сетчатки в фовеа составляла от 430 до 840 мкм, в среднем 645±126 мкм.
Острота зрения у пациентов основной группы в глазах с непролиферативной ДР была в пределах от 0,05 до 0,3 с/к; с пролиферативной ретинопатией - от светоощущения с правильной проекцией света до 0,2 с/к. Средний уровень внутриглазного давления составлял 21±2,3 мм рт. ст. (от 18 до 26 мм рт. ст.).
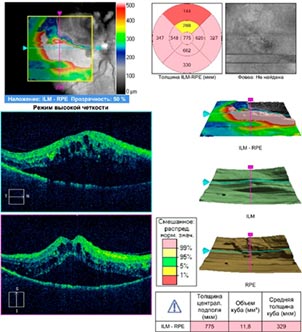
Рис. 5. Оптическая когерентная томография макулы правого глаза пациентки Ж. Высокий макулярный отек, высокая и распространенная отслойка нейроэпителия, кистозные изменения сетчатки
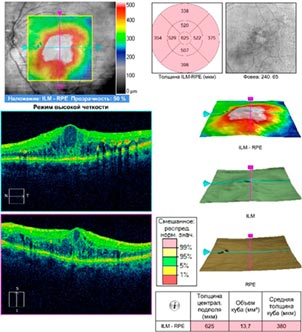
Рис. 6. Оптическая когерентная томография макулы левого глаза пациентки А. Макулярный отек, кистозные изменения сетчатки, отложения "твердых экссудатов"
В группе сравнения у всех 40 пациентов (40 глаз) имел место диффузный ДМО. В 28 глазах (70 %) отмечалась локальная ОНЭ, в 30 глазах (75 %) отек имел кистозный характер.
Острота зрения у пациентов группы сравнения в глазах с ППДР до начала лечения была в пределах от 0,04 до 0,5 с/к; с ПДР - от 0,01 с/к до 0,4 с/к. Средний уровень внутриглазного давления составлял 20±2,6 мм рт. ст. (от 16 до 24 мм рт. ст.).
| Группа | Количество глаз | Локальная отслойка нейроэпителия, глаз (%) | Кистозный диабетический макулярный отек, глаз (%) |
|---|---|---|---|
| Основная | 38 | 20 (53) | 22 (58) |
| Сравнения | 40 | 28 (70) | 30 (75) |
В основной группе в 10 глазах с ППДР для достижения регресса ДМО были выполнены 3 интравитреальные инъекции луцентиса, в 8 глазах - 6 инъекций, в среднем - 4,3 инъекций/глаз. У пациентов с ПДР в 10 глазах было выполнено 6 интравитреальных инъекций луцентиса, в 8 глазах - 8 инъекций, в 2 глазах - 10 инъекций, в среднем - 7,2 инъекций/глаз. В среднем пациентам основной группы было произведено 5,8 инъекций/глаз. Таким образом, у пациентов основной группы с ДМО на фоне ППДР среднее количество инъекций луцентиса было значимо меньше, чем у пациентов с ПДР: 4,3 против 7,2 соответственно (p=0,003) (табл. 2).
В подгруппе пациентов с ППДР и макулярным отеком с ОНЭ (10 глаз) в 8 глазах потребовались 3 инъекции луцентиса, в 2 глазах - 6 инъекций, в среднем - 3,6 инъекций/глаз. У всех пациентов с ПДР и макулярным отеком с ОНЭ (10 глаз) для достижения регресса отека потребовались 6 инъекций/глаз. У пациентов основной группы с макулярным отеком и отсутствием ОНЭ в среднем были проведены 6,8 инъекций/глаз: у пациентов с ППДР - 5 инъекций/глаз, с ПДР - 8,4 (табл. 2).
Название рукописи (статьи): "Анализ эффективности анти-VEGF терапии диабетического макулярного отёка в авитричных глазах"
| Группа | Морфология диабетического макулярного отека | Препролиферативная диабетическая ретинопатия | Пролиферативная диабетическая ретинопатия | Препролиферативная диабетическая ретинопатия + пролиферативная диабетическая ретинопатия |
|---|---|---|---|---|
| Основная | Отслойка нейроэпителия + Нет отслойки нейроэпителия | 4,3 | 7,2 | 5,8 |
| Отслойка нейроэпителия | 3,6 | 6,0 | 4,8 | |
| Нет отслойки нейроэпителия | 5 | 8,4 | 6,8 | |
| Сравнения | Отслойка нейроэпителия + Нет отслойки нейроэпителия | 4,2 | 7,0 | 5,6 |
| Отслойка нейроэпителия | 3,8 | 5,7 | 4,7 | |
| Нет отслойки нейроэпителия | 4,6 | 8,3 | 6,5 |
Таким образом, количество инъекций у пациентов основной группы с макулярным отеком и ОНЭ значимо отличалось от среднего количества инъекций при отсутствии ОНЭ (4,8 против 6,8 соответственно, p=0,012).
Через 1 месяц после завершения анти-VEGF терапии острота зрения пациентов основной группы повысилась в среднем на 0,2±0,12 (от 0,05 до 0,3) у пациентов с ППДР и на 0,1±0,05 (от 0,02 до 0,2) у пациентов с ПДР.
По данным ОКТ, макулярный отек регрессировал полностью в 28 глазах (74 %) - толщина сетчатки уменьшилась на 340-460 мкм, в среднем на 380±37 мкм. В 10 глазах пациентов с ПДР, кистозным характером отека и отсутствием ОНЭ, толщина сетчатки уменьшилась до 310-360 мкм (в среднем до 335±17 мкм) на 280-350 мкм (в среднем на 315±22 мкм). Помимо этого, изменилась морфология отека - уменьшились высота и количество интраретинальных кист, то есть отмечался частичный регресс макулярного отека. В глазах с частичным регрессом отека впоследствии была проведена дополнительная лазеркоагуляция сетчатки.
В группе сравнения для достижения регресса макулярного отека в 12 глазах с ППДР были выполнены 3 интравитреальные инъекции луцентиса, в 8 глазах - 6 инъекций, в среднем 4,2 инъекций/глаз. Разница с основной группой была незначимая (p=0,905). У пациентов группы сравнения с ПДР в 4 глазах были выполнены 4 интравитреальных инъекции луцентиса, в 6 глазах - 6 инъекций, в 4 глазах - 8 инъекций, в 4 глазах - 9 инъекций, в 2 глазах - 10 инъекций. В среднем это составило 7,0 инъекций/глаз. Разница с основной группой также оказалась незначимой (p=0,971). Пациентам группы сравнения в среднем было произведено 5,6 инъекций/глаз, что не имело значимых отличий от основной группы (p=0,723). У пациентов группы сравнения с макулярным отеком на фоне ППДР среднее количество инъекций луцентиса, так же как и в основной группе, было значимо меньше, чем у пациентов с ПДР: 4,2 против 7,0 (p=0,005).
При наличии ОНЭ на фоне макулярного отека у пациентов группы сравнения, так же, как и в основной группе, потребовалось меньшее количество инъекций луцентиса, в сравнении с глазами с ее отсутствием. В подгруппе пациентов с ППДР и макулярным отеком с ОНЭ (16 глаз) в 12 глазах потребовались 3 инъекции луцентиса, в 4 глазах - 6 инъекций, в среднем - 3,8 инъекций/глаз. У пациентов с ПДР и макулярным отеком с ОНЭ (12 глаз) для достижения регресса отека в 4 глазах потребовались 4 инъекции, в 6 глазах - 6 инъекций, в 2 глазах - 8 инъекций, в среднем - 5,7 инъекций/глаз (p=0,029). При отсутствии ОНЭ у пациентов группы сравнения в среднем было проведено 6,5 инъекций/глаз: у пациентов с ППДР - 4,6, с ПДР - 8,3. В среднем у пациентов группы сравнения с макулярным отеком и ОНЭ было произведено 4,7 инъекций/глаз, что значимо отличается от среднего количества инъекций при отсутствии ОНЭ - 6,5 инъекций/глаз (p=0,019).
Через 1 месяц после завершения анти-VEGF терапии острота зрения пациентов группы сравнения повысилась в среднем на 0,15±0,1 (от 0,05 до 0,3) у пациентов с ППДР и на 0,2±0,1 (от 0,01 до 0,3) у пациентов с ПДР. По данным ОКТ, в группе сравнения макулярный отек регрессировал полностью в 30 глазах (75 %) - толщина сетчатки уменьшилась на 330-475 мкм, в среднем на 398±41 мкм.
В 10 глазах пациентов группы сравнения с ПДР, кистозным отеком и отсутствием ОНЭ, толщина сетчатки уменьшилась до 310-360 мкм (в среднем до 338±15 мкм) на 270-345 мкм (в среднем на 330±16 мкм), уменьшились высота и количество интраретинальных кист. В глазах с частичным регрессом отека впоследствии также была проведена дополнительная лазеркоагуляция сетчатки.
Полученные нами данные показывают, что отсутствие нативного стекловидного тела после эндовитреального вмешательства (авитрия) не препятствует лечебному действию луцентиса при его интравитреальном введении. Полный регресс ДМО в авитричных глазах произошел в 74 % случаев; в глазах с нативным стекловидным телом - в 75 % случаев. Среднее количество интравитреальных инъекций луцентиса у пациентов с авитрией составило 5,8; у пациентов с нативным стекловидным телом - 5,6 (p=0,723). Это соответствует данным литературы.
Несмотря на то, что, по мнению ряда авторов, в авитричном глазу луцентис быстро резорбируется, не оказывая должного эффекта, результаты исследований на животных моделях показывают противоположные результаты. При изучении фармакокинетики ранибизумаба в витричных и авитричных глазах кролика были показаны сходные фармакокинетические свойства луцентиса в обеих группах [13].
Bressler S.B. с соавторами показали, что изменения остроты зрения и толщины фовеалярной сетчатки, по сравнению с исходным уровнем, а также количество инъекций ранибизумаба и сеансов лазеркоагуляции сетчатки сопоставимы в глазах с авитрией и нативным стекловидным телом. Авторы отмечают более медленное улучшение показателей ОКТ в течение первого года терапии в авитричных глазах [16].
Ряд авторов показывают влияние морфологии ДМО на успешность анти-VEGF терапии. Положительными прогностическими критериями считаются наличие локальной ОНЭ, исходная большая толщина хориоидеи [18, 26, 27].
В нашем исследовании при наличии отслойки нейроэпителия на фоне макулярного отека в большинстве случаев потребовалось меньшее количество инъекций луцентиса, в сравнении с глазами с ее отсутствием как при ППДР, так и при ПДР. У пациентов с нативным стекловидным телом с макулярным отеком и ОНЭ были произведены 4,7 инъекций/глаз, в сравнении с 6,5 инъекций/глаз в глазах с отсутствием ОНЭ; в глазах с авитрией количество инъекций/глаз составило 4,8 в сравнении с 6,8 соответственно (p=0,012).
Следует отметить, что при проведении анти-VEGF терапии в авитричных глазах существует риск развития гемофтальма в отдаленном периоде. Субтотальный гемофтальм произошёл в 5 глазах (13 %) 4 пациентов основной группы через 12-14 месяцев после интравитреального введения луцентиса. В связи с отсутствием положительной динамики на фоне консервативной рассасывающей терапии гемофтальма, на 3 глазах было произведено повторное эндовитреальное вмешательство с тампонадой силиконовым маслом с лечебной и социально-адаптационной целью. На 2 глазах гемофтальм регрессировал на фоне консервативного лечения. У пациентов группы сравнения в ближайшие и отдаленные сроки после завершения анти-VEGF терапии геморрагические осложнения не отмечались.
Другой особенностью оказалась более длительная послеоперационная реакция авитричных глаз после интравитреального введения луцентиса. Ее продолжительность составила до 10-14 дней, в сравнении с 1-3 днями в глазах с нативным стекловидным телом. Купирование послеоперационной реакции у 10 пациентов с авитрией (29 %) потребовало назначения инстилляций нестероидных противовоспалительных препаратов. Подобные проявления, вероятно, были связаны с периодической травматизацией области цилиарного тела при выполнении интравитреальных инъекций на фоне длительного пролиферативного процесса в области базиса стекловидного тела, обусловленного удалением стекловидного тела при эндовитреальном вмешательстве.
Выводы
|
 |
 |
1. Эффективность интравитреального введения луцентиса при лечении ДМО сопоставима в глазах с нативным стекловидным телом и авитрией.
2. Полный регресс ДМО в авитричных глазах произошел в 74 % случаев, в глазах с нативным стекловидным телом - в 75 % случаев. Среднее количество интравитреальных инъекций луцентиса у пациентов авитрией составило 5,8 на глаз, у пациентов с нативным стекловидным телом - 5,6 на глаз.
3. У пациентов с ДМО на фоне ППДР количество интравитреальных введений луцентиса было значимо меньше, чем при ПДР.
4. Наличие локальной ОНЭ на фоне диффузного макулярного отека является прогностически благоприятным фактором для проведения анти-VEGF терапии.
5. Особенностью интравитреального введения луцентиса в авитричных глазах является возможность развития поздних геморрагических осложнений и более длительная послеоперационная воспалительная реакция.
Литература |
 |
 1. Балашевич Л.И., Измайлов А.С. Глазные проявления диабета. - СПб.: Спб. МАПО. - 2004.
1. Балашевич Л.И., Измайлов А.С. Глазные проявления диабета. - СПб.: Спб. МАПО. - 2004. 2. Бикбов М.М., Файзрахманов Р.Р., Зайнулин Р.М., Зайнетдинов А.Ф., Гильманшин Т.Р., Каланов М.Р. Макулярный отек как проявление диабетической ретинопатии // Сахарный диабет. - 2017. - Т. 20, № 4. - С. 263-269.
2. Бикбов М.М., Файзрахманов Р.Р., Зайнулин Р.М., Зайнетдинов А.Ф., Гильманшин Т.Р., Каланов М.Р. Макулярный отек как проявление диабетической ретинопатии // Сахарный диабет. - 2017. - Т. 20, № 4. - С. 263-269.  3. Борискина Л.Н., Потапова В.Н. Современные методы лечения рецидивирующего гемофтальма и диабетического макулярного отека при пролиферативной диабетической ретинопатии на примере клинического случая // Практическая медицина. - 2012. - № 4-2. - С. 88-91.
3. Борискина Л.Н., Потапова В.Н. Современные методы лечения рецидивирующего гемофтальма и диабетического макулярного отека при пролиферативной диабетической ретинопатии на примере клинического случая // Практическая медицина. - 2012. - № 4-2. - С. 88-91.  4. Злобин И.В., Алпатов С.А. Эффективность интравитреального введения ранибизумаба в лечении пациентов с диабетическим макулярным отеком // Acta Biomedica Scientifica. - 2011. - № 3-1. - С. 38-43.
4. Злобин И.В., Алпатов С.А. Эффективность интравитреального введения ранибизумаба в лечении пациентов с диабетическим макулярным отеком // Acta Biomedica Scientifica. - 2011. - № 3-1. - С. 38-43.  5. Кирилюк М.Л. Медикаментозное лечение и профилактика диабетической ретинопатии при сахарном диабете типа 1. Обзор литературы и клинических исследований // Международный эндокринологический журнал. - 2012. - Т. 8, № 5. - С. 70-75.
5. Кирилюк М.Л. Медикаментозное лечение и профилактика диабетической ретинопатии при сахарном диабете типа 1. Обзор литературы и клинических исследований // Международный эндокринологический журнал. - 2012. - Т. 8, № 5. - С. 70-75.  6. Нероев В.В. Современные аспекты лечения диабетического макулярного отека // Российский офтальмологический журнал. - 2012. - Т. 5, № 1. - С. 4-7.
6. Нероев В.В. Современные аспекты лечения диабетического макулярного отека // Российский офтальмологический журнал. - 2012. - Т. 5, № 1. - С. 4-7.  7. Сорокин Е.Л., Коленко О.В., Московченко А.А., Пшеничнов М.В. Доля диффузных макулярных отеков у пациентов с сахарным диабетом 2 типа при первичном обращении в отдел лазерной хирургии // Современные технологии в офтальмологии. - 2014. - № 2. - С. 81-83.
7. Сорокин Е.Л., Коленко О.В., Московченко А.А., Пшеничнов М.В. Доля диффузных макулярных отеков у пациентов с сахарным диабетом 2 типа при первичном обращении в отдел лазерной хирургии // Современные технологии в офтальмологии. - 2014. - № 2. - С. 81-83.  8. Сорокин Е.Л., Пшеничнов М.В. Значение морфометрических параметров сетчатки в прогнозировании диабетического макулярного отека у больных сахарным диабетом 2 типа // Сахарный диабет. - 2008. - № 3. - С. 18-19.
8. Сорокин Е.Л., Пшеничнов М.В. Значение морфометрических параметров сетчатки в прогнозировании диабетического макулярного отека у больных сахарным диабетом 2 типа // Сахарный диабет. - 2008. - № 3. - С. 18-19.  9. Фокин В.П., Борискина Л.Н., Потапова В.Н., Полякова В.Р. Анализ эффективности комбинированного метода лечения при диабетическом макулярном отёке // Вестник Новосибирского государственного университета. Серия: Биология, клиническая медицина. - 2011. - Т. 9, № 4. - С. 43-47.
9. Фокин В.П., Борискина Л.Н., Потапова В.Н., Полякова В.Р. Анализ эффективности комбинированного метода лечения при диабетическом макулярном отёке // Вестник Новосибирского государственного университета. Серия: Биология, клиническая медицина. - 2011. - Т. 9, № 4. - С. 43-47.  10. Шадричев Ф.Е., Шкляров Е.Б., Григорьева Н.Н. Использование анти-VEGF терапии в лечение диабетического макулярного отека // Офтальмологические ведомости. - 2011. - Т. 4, № 1. - С. 83-93.
10. Шадричев Ф.Е., Шкляров Е.Б., Григорьева Н.Н. Использование анти-VEGF терапии в лечение диабетического макулярного отека // Офтальмологические ведомости. - 2011. - Т. 4, № 1. - С. 83-93.  11. Шишкин М.М., Бабаева Д.Б., Шиковная Е.Ю. Пролиферативная диабетическая ретинопатия с витреопапиллярным тракционным компоненты: особенности клиники и результаты лечения // Современные технологии в офтальмологии. - 2015. - № 1. - С. 133.
11. Шишкин М.М., Бабаева Д.Б., Шиковная Е.Ю. Пролиферативная диабетическая ретинопатия с витреопапиллярным тракционным компоненты: особенности клиники и результаты лечения // Современные технологии в офтальмологии. - 2015. - № 1. - С. 133.  12. Шишкин М.М., Юлдашева Н.М., Шиковная Е.Ю. Особенности двухэтапной хирургии у пациентов с пролиферативной диабетической ретрнопатией и катарактой // Практическая медицина. - 2012. - № 4-2. - С. 149-150.
12. Шишкин М.М., Юлдашева Н.М., Шиковная Е.Ю. Особенности двухэтапной хирургии у пациентов с пролиферативной диабетической ретрнопатией и катарактой // Практическая медицина. - 2012. - № 4-2. - С. 149-150.  13. Ahn S.J., Ahn J., Park S., Kim H., Hwang D.J., Park J.H., Park J.Y., Chung J.Y., Park K.H., Woo S.J. Intraocular pharmacokinetics of ranibizumab in vitrectomized versus nonvitrectomized eyes // Invest. Ophthalmol. Vis. Sci. - 2014. - Vol. 55, № 1. - P. 567-573.
13. Ahn S.J., Ahn J., Park S., Kim H., Hwang D.J., Park J.H., Park J.Y., Chung J.Y., Park K.H., Woo S.J. Intraocular pharmacokinetics of ranibizumab in vitrectomized versus nonvitrectomized eyes // Invest. Ophthalmol. Vis. Sci. - 2014. - Vol. 55, № 1. - P. 567-573.  14. Antcliff R.J., Marshall J. The pathogenesis of edema in diabetic maculopathy // Semin Ophthalmol. - 1999. - Vol. 14, № 4. - P. 223-232.
14. Antcliff R.J., Marshall J. The pathogenesis of edema in diabetic maculopathy // Semin Ophthalmol. - 1999. - Vol. 14, № 4. - P. 223-232.  15. Bhagat N., Grigorian R., Tutela A., Zarbin M. Diabetic macular edema: pathogenesis and treatment // Survey of ophthalmology. - 2009. - Vol. 54, № 1. - P. 1-32.
15. Bhagat N., Grigorian R., Tutela A., Zarbin M. Diabetic macular edema: pathogenesis and treatment // Survey of ophthalmology. - 2009. - Vol. 54, № 1. - P. 1-32.  16. Bressler S.B., Melia M., Glassman A.R., Almukhtar T., Jampol L.M., Shami M., Berger B.B., Bressler N.M. Ranibizumab plus prompt or deferred laser for diabetic macular edema in eyes with vitrectomy before anti-vascular endothelial growth factor therapy // Retina. - 2015. - Vol. 35, № 12. - P. 2516-2528.
16. Bressler S.B., Melia M., Glassman A.R., Almukhtar T., Jampol L.M., Shami M., Berger B.B., Bressler N.M. Ranibizumab plus prompt or deferred laser for diabetic macular edema in eyes with vitrectomy before anti-vascular endothelial growth factor therapy // Retina. - 2015. - Vol. 35, № 12. - P. 2516-2528.  17. Chune D.W., Heier J.S., Topping T.M., Duker J.S., Bankert J.M. A pilot study of multiple intravitreal injections of ranibizumab in patients with center-involving clinically significant diabetic macular edema // Ophthalmology. - 2006. - Vol. 113, № 10. - P. 1706-1712.
17. Chune D.W., Heier J.S., Topping T.M., Duker J.S., Bankert J.M. A pilot study of multiple intravitreal injections of ranibizumab in patients with center-involving clinically significant diabetic macular edema // Ophthalmology. - 2006. - Vol. 113, № 10. - P. 1706-1712.  18. Gerendas B., Simader C., Deak G.G., Prager S.G., Lammer J., Waldstein S.M., Kundi M., Schmidt-Erfurth U. Morphological parameters relevant for visual and anatomic outcomes during anti-VEGF therapy of diabetic macular edema in the RESTORE trial // Invest. Ophthalmol. Vis. Sci. - 2014. - Vol. 55, № 13. - P. 1971.
18. Gerendas B., Simader C., Deak G.G., Prager S.G., Lammer J., Waldstein S.M., Kundi M., Schmidt-Erfurth U. Morphological parameters relevant for visual and anatomic outcomes during anti-VEGF therapy of diabetic macular edema in the RESTORE trial // Invest. Ophthalmol. Vis. Sci. - 2014. - Vol. 55, № 13. - P. 1971.  19. Klein R., Klein B.E., Moss S.E., Cruickshanks K.J. The Wisconsin Epidemiologic Study of Diabetic Retinopathy: XVII. The 14-year incidence and progression of diabetic retinopathy and associated risk factors in type 1 diabetes // Ophthalmology. - 1998. - Vol. 105, № 10. - P. 1801-1815.
19. Klein R., Klein B.E., Moss S.E., Cruickshanks K.J. The Wisconsin Epidemiologic Study of Diabetic Retinopathy: XVII. The 14-year incidence and progression of diabetic retinopathy and associated risk factors in type 1 diabetes // Ophthalmology. - 1998. - Vol. 105, № 10. - P. 1801-1815. 20. Klein R., Lee K.E., Gangnon R.E., Klein B.E. The 25-Year Incidence of Visual Impairment in Type 1 Diabetes // Ophthalmology. - 2010. - Vol. 117, № 1. - P. 63-70.
20. Klein R., Lee K.E., Gangnon R.E., Klein B.E. The 25-Year Incidence of Visual Impairment in Type 1 Diabetes // Ophthalmology. - 2010. - Vol. 117, № 1. - P. 63-70.  21. Massin P., Bandello F., Garweg J.G., Hansen L.L., Harding S.P., Larsen M., Mitchell P., Sharp D., Wolf-Schnurrbusch U.E., Gekkieva M., Weichselberger A., Wolf S. Safety and efficacy of ranibizumab in diabetic macular edema (RESOLVE Study). A 12-month, randomized, controlled, double-masked, multicenter phase II study // Diabetes care. - 2010. - Vol. 33, № 11. - P. 2399-2405.
21. Massin P., Bandello F., Garweg J.G., Hansen L.L., Harding S.P., Larsen M., Mitchell P., Sharp D., Wolf-Schnurrbusch U.E., Gekkieva M., Weichselberger A., Wolf S. Safety and efficacy of ranibizumab in diabetic macular edema (RESOLVE Study). A 12-month, randomized, controlled, double-masked, multicenter phase II study // Diabetes care. - 2010. - Vol. 33, № 11. - P. 2399-2405.  22. Mitchell P., Bandello F., Schmidt-Erfurth U., Lang G.E., Massin P., Schlingemann R.O., Sutter F., Simader C., Burian G., Gerstner O., Weichselberger A. The RESTORE study: ranibizumab monotherapy or combined with laser versus laser monotherapy for diabetic macular edema // Ophthalmology. - 2011. - Vol. 118, № 4. - P. 615-625.
22. Mitchell P., Bandello F., Schmidt-Erfurth U., Lang G.E., Massin P., Schlingemann R.O., Sutter F., Simader C., Burian G., Gerstner O., Weichselberger A. The RESTORE study: ranibizumab monotherapy or combined with laser versus laser monotherapy for diabetic macular edema // Ophthalmology. - 2011. - Vol. 118, № 4. - P. 615-625.  23. Muether P.S., Droege K.M., Fauser S. Vascular endothelial growth factor suppression times in patients with diabetic macular oedema treated with ranibizumab // British Journal of Ophthalmology. - 2014. - Vol. 98, № 2. - P. 179-181.
23. Muether P.S., Droege K.M., Fauser S. Vascular endothelial growth factor suppression times in patients with diabetic macular oedema treated with ranibizumab // British Journal of Ophthalmology. - 2014. - Vol. 98, № 2. - P. 179-181.  24. Nakamura S., Iwasaki N., Funatsu H., Kitano S., Iwamoto Y. Impact of variants in the VEGF gene on progression of proliferative diabetic retinopathy // Graefes Arch Clin Exp Ophthalmol. - 2009. - Vol. 247, No. 1. - P. 21-26.
24. Nakamura S., Iwasaki N., Funatsu H., Kitano S., Iwamoto Y. Impact of variants in the VEGF gene on progression of proliferative diabetic retinopathy // Graefes Arch Clin Exp Ophthalmol. - 2009. - Vol. 247, No. 1. - P. 21-26.  25. PrÜnte C., Fajnkuchen F., Mahmood S., Ricci F., Hatz K., Studnička J., Bezlyak V., Parikh S., Stubbings W.J., Wenzel A., Figueira J. Ranibizumab 0.5 mg treat-and-extend regimen for diabetic macular oedema: the RETAIN study // British Journal of Ophthalmology. - 2016. - Vol. 100, № 6. - P. 787-795.
25. PrÜnte C., Fajnkuchen F., Mahmood S., Ricci F., Hatz K., Studnička J., Bezlyak V., Parikh S., Stubbings W.J., Wenzel A., Figueira J. Ranibizumab 0.5 mg treat-and-extend regimen for diabetic macular oedema: the RETAIN study // British Journal of Ophthalmology. - 2016. - Vol. 100, № 6. - P. 787-795.  26. Rayess N., Rahimy E., Ying G.S., Bagheri N., Ho A.C., Regillo C.D., Vander J.F., Hsu J. Baseline choroidal thickness as a predictor for response to anti-vascular endothelial growth factor therapy in diabetic macular edema // American Journal of Ophthalmology. - 2015. - Vol. 159, № 1. - P. 85-91.
26. Rayess N., Rahimy E., Ying G.S., Bagheri N., Ho A.C., Regillo C.D., Vander J.F., Hsu J. Baseline choroidal thickness as a predictor for response to anti-vascular endothelial growth factor therapy in diabetic macular edema // American Journal of Ophthalmology. - 2015. - Vol. 159, № 1. - P. 85-91.  27. Romero-Aroca P. Targeting the pathophysiology of diabetic macular edema // Diabetes care. - 2010. - Vol. 33, № 11. - P. 2484-2485.
27. Romero-Aroca P. Targeting the pathophysiology of diabetic macular edema // Diabetes care. - 2010. - Vol. 33, № 11. - P. 2484-2485.  28. White N.H., Sun W., Cleary P.A., Tamborlane W.V., Danis R.P., Hainsworth D.P., Davis M.D. Effect of prior intensive therapy in type 1 diabetes on 10-year progression of retinopathy in the DCCT/EDIC: comparison of adults and adolescents // Diabetes. - 2010. - Vol. 59, № 5. - P. 1244-1253.
28. White N.H., Sun W., Cleary P.A., Tamborlane W.V., Danis R.P., Hainsworth D.P., Davis M.D. Effect of prior intensive therapy in type 1 diabetes on 10-year progression of retinopathy in the DCCT/EDIC: comparison of adults and adolescents // Diabetes. - 2010. - Vol. 59, № 5. - P. 1244-1253.
 |
Главное меню |
 |
Заглавие |
 |
Введение |
 |
Материалы и методы |
 |
Результаты и обсуждение |
 |
Выводы |
 |
Литература |
Оригинальная верстка  |
|
Телефон: (4212) 76-13-96
«Дальневосточный медицинский журнал»