2021 год № 3
Обмен опытом
Резюме:
Ключевые слова:
Summary:
Key words:
Введение |
 |
 |
Врожденные пороки сердца (ВПС) достаточно распространенная патология среди заболеваний сердечно-сосудистой системы, которая является одной из основных причин смерти детей первого года жизни. Удельный вес всех ВПС в России (с учетом случаев внутриутробной смерти плода и ранних выкидышей) среди врожденных пороков развития достигает 40 %. ВПС является причиной не менее 11 % младенческих смертей и составляет около 50 % от всех случаев смерти, ассоциирующихся с пороками развития [5].
В числе ВПС встречается один из сложных пороков - открытый атриовентрикулярный канал, частота которого составляет 4,21 на 10 000 человек [6]. Эта аномалия может сочетаться с пороками конотрункуса (аномалии развития артериальных конусов, аорты, легочного ствола).
К порокам конотрункуса относится редкий врожденный порок - двойное отхождение магистральных сосудов (аорты и легочного ствола) из правого желудочка (ДОСПЖ). Это группа врожденных пороков сердца, характеризующаяся аномальным типом вентрикуло-артериальной связи, при которой аорта и легочный ствол полностью или преимущественно происходят от правого желудочка [4, 10], возникающей вследствие нарушения ротации конуса и его вклинения между атриовентрикулярными клапанами [9] и сопровождающейся нарушением формирования выхода из левого желудочка [1, 2]. Частота порока по клиническим данным составляет 0,72 % [4], а по патологоанатомическим - 2,7 % [2,4]. Доля оперативных вмешательств по поводу ДОСПЖ среди всех врожденных пороков сердца в России составляет 1,55 % при средней летальности 9,96 % [3]. В целом медиана выживаемости не превышает 5 лет [8] и без оперативного лечения до 15 лет доживают лишь 17,1 % больных со всеми типами ДОСПЖ [7]. А сочетание двойного отхождения сосудов из правого желудочка с общим атриовентрикулярным каналом относится к "сложным формам" ДОСПЖ, и являются крайне тяжелыми ВПС [4].
Тот факт, что такие сочетания встречаются редко, затрудняет изучение порока и не позволяет накопить достаточный опыт для диагностики и хирургической коррекции порока. Поэтому, роль морфологов состоит в предоставлении детальных сведений при сложных сердечных аномалиях.
Цель работы - выявить особенности строения камер и предсердно-желудочковых клапанов сердца при сочетании открытого атриовентрикулярного канала с двойным отхождением магистральных сосудов из правого желудочка. Выявить особенности кровоснабжения стенок камер сердца и венозного оттока.
Материалы и методы
|
 |
 |
Авторы описали препарат сердца ребенка с болезнью Дауна в возрасте 9 месяцев, умершего в связи с наличием сложного врожденного порока сердца сочетанием ДОСПЖ с открытым атриовентрикулярным каналом. Использованы традиционные методы анатомического препарирования сосудов. Методом описательной анатомии исследовали топографию магистральных сосудов, особенности строения предсердно-желудочковых клапанов, мясистых трабекул, топографию устьев венечных артерий и магистральных стволов, тип ветвления артериальных сосудов, угол отхождения ветвей. Описывали истоки сердечных вен, устанавливали их зоны дренирования. Обращали внимание на местоположение венечного синуса.
Результаты и обсуждение
|
 |
 |
Анатомической особенностью порока в данном случае является то, что передняя створка правого предсердно-желудочкового клапана контактирует с фиброзным кольцом аорты, а ее расщепленная часть через дефект межжелудочковой перегородки перебрасывается в левый желудочек и соединяется с расщепленной передней створкой левого предсердно-желудочкового клапана. Выход из полости левого желудочка осуществляется через дефект межжелудочковой перегородки и ограничен краем дефекта и нижними поверхностями этих створок, которые выводят к аортальному устью, находящемуся в полости правого желудочка в области его основания (рис. 1). При этом, устье аорты ограничивается задней поверхностью наджелудочкового гребня и дополнительно еще расщепленной перегородочной створкой правого предсердно-желудочкового клапана. Присутствие наджелудочкового гребня обеспечивает выход из полости правого желудочка в артериальный конус и далее в устье легочного ствола. Мышечные трабекулы на стенках камеры крупно- и среднепетлистые, имеют косое направление, а в области верхушки поперечное. Между ними располагаются сухожильные нити. Перегородочно-краевая трабекула лежит на межжелудочковой перегородке и в нижнем отделе своим телом внедряется в переднюю стенку правого желудочка, ограничивая этим самым выход из приточного отдела в артериальный конус. От нее ответвляется крупная мышечная трабекула, которая соединяется с основанием передней сосочковой мышцы, а затем поднимается кверху и формирует нижний край дефекта межжелудочковой перегородки. Передняя ножка перегородочно-краевой трабекулы принимает участие в образовании конусной перегородки, а ее задняя ножка ограничивает край дефекта. От задней поверхности наджелудочкового гребня в месте окончания задней ножки отходит сосочковая мышца, высотой 2 мм, а от нее ответвляются три крупные сухожильные хорды, идущие на соединение с передней створкой правого предсердно-желудочкового клапана. Передняя сосочковая мышца располагалась при этом на передней стенке правого желудочка, а рядом с ней на межжелудочковой перегородке находилась перегородочная сосочковая мышца. От них отходили сухожильные нити как к передней, так и задней створкам клапана. Наряду с этим тонкие сосочковые мышцы (с диаметром основания 1 мм) располагались на задней стенке правого желудочка и межжелудочковой перегородке. Их сухожильные хорды вплетались в перегородочную и заднюю створки правого предсердно-желудочкового клапана. В левом желудочке сосочковые мышцы располагались на его передней и задней стенках, а их сухожильные нити соединялись с частями расщепленной передней створки и с задней створкой левого предсердно-желудочкового клапана.
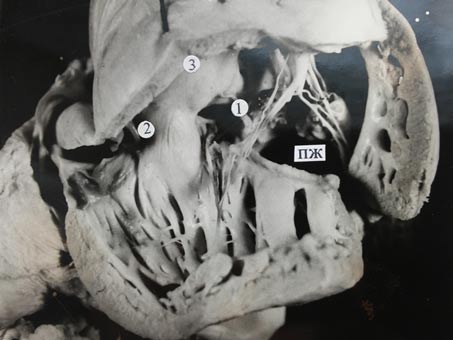
Рис. 1. Препарат сердца с открытым атриовентрикулярным каналом в сочетании с двойным отхождением магистральных сосудов из правого желудочка: 1 - устье аорты; 2 - устье легочного ствола;3 - артериальный конус
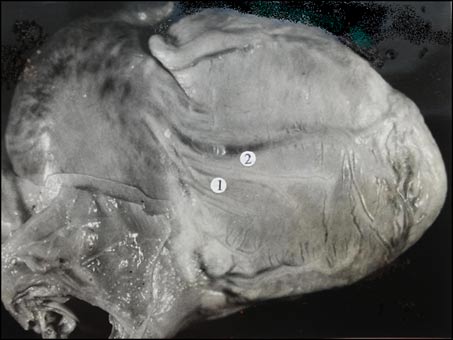
Рис. 2. Препарат сердца с открытым атриовентрикулярным каналом в сочетании с двойным отхождением магистральных сосудов из правого желудочка: 1 - правая венечная артерия; 2 - средняя вена сердца
Кровоснабжение сердца осуществлялось двумя венечными артериями. Устье левой венечной артерии находилось в левом аортальном синусе на уровне верхнего края полулунной заслонки. Ее основной ствол появлялся из-под легочного ствола, имея длину 10 мм, затем он следовал к основанию левого ушка, после чего делился на переднюю межжелудочковую и огибающую ветви.
Передняя межжелудочковая ветвь ложилась в одноименную борозду, ветвилась по рассыпному типу, давая артериальные сосуды более крупного калибра к передней стенке левого желудочка и к межжелудочковой перегородке, а ветви малого калибра в основном отходили от нее к передней стенке правого желудочка. Затем она огибала сердечную вырезку и заканчивалась в верхушечной части задних стенок желудочковых камер. Огибающая ветвь следовала по венечной борозде, ветвилась по рассыпному типу и кровоснабжала на своем пути стенки левого предсердия и левого желудочка до задней межжелудочковой борозды.
Устье правой венечной артерии находилось в правом аортальном синусе на уровне края полулунной заслонки. Сразу от устья отходила артерия конуса крупного калибра. Она ветвилась на передней стенке конуса и правого желудочка. Основной ствол правой венечной артерии следовал по венечной борозде к правому краю сердца и ветвился по магистральному типу, отдавая два сосуда крупного калибра к передней стенке правого желудочка, а на диафрагмальной поверхности к задней стенке отходила крупная ветвь, которая спускалась книзу рядом с правым краем сердца. Ее ветви малого калибра кровоснабжали стенки правого предсердия. Затем, правая венечная артерия, не доходя до задней межжелудочковой борозды, делилась на два сосуда, один из которых спускался косо вниз по задней стенке правого желудочка, кровоснабжая его миокард и задние отделы межжелудочковой перегородки. Второй артериальный сосуд по венечной борозде направлялся к задней стенке левого желудочка, где и заканчивался своими конечными ветвями преимущественно в верхнем отделе камеры.
Большая вена сердца своими истоками начиналась у верхушки сердца, затем она поднималась кверху в передней межжелудочковой борозде и принимала ряд венозных сосудов разного калибра от передних стенок желудочков и межжелудочковой перегородки. В области основания левого желудочка ее ствол отклонялся влево, ложился в венечную борозду и достигал венечного синуса, принимая на своем пути мелкие венозные сосуды от стенок левого предсердия и левого желудочка.
Средняя вена сердца имела большую зону дренирования. Ее истоки начинались на передней стенке верхушечного отдела правого желудочка, а сформировавшийся ствол огибал сердечную вырезку и ложился в заднюю межжелудочковую борозду. Следуя по ней, средняя вена сердца принимала множество венозных сосудов разного калибра от задних стенок желудочковых камер и впадала в венечный синус в области его устья.
Задняя вена левого желудочка имела обычную зону дренирования. Ее корни располагались у верхушки сердца. Далее своим основным стволом она следовала косо кверху по задней стенке левого желудочка, принимала ряд венозных сосудов разного калибра и входила в венечный синус.
Две передние вены сердца имели большую зону дренирования, своими истоками начинались в нижнем отделе передней стенки правого желудочка и поднимались кверху параллельно друг к другу к венечной борозде, принимая множество мелких венозных сосудов от миокарда камеры, после чего самостоятельными устьями впадали в полость правого предсердия на уровне его боковой стенки. Малая вена сердца не обнаружена.
Венечный синус имел длину 10,5 мм, его диаметр перед устьем по длинной оси достигал 6 мм, а по короткой - 3 мм. Форма синуса напоминала уплощенный изгибающийся конус, расположившийся выше венечной борозды на стенке левого предсердия. Заслонка устья венечного синуса отсутствовала.
Анатомические особенности данного порока необходимо учитывать при его коррекции. Особенностью кровоснабжения в данном случае было преобладание бассейна правой венечной артерии над бассейном левой. Венозный отток крови осуществлялся через подэпикардиальные вены, среди которых средняя вена и передние вены сердца имели большую зону дренирования, а большая вена сердца и задняя вена левого желудочка с обычной зоной дренирования направляли кровь в венечный синус.
Литература |
 |
 1. Банкл Г. Врожденные пороки сердца и крупных сосудов: Пер. с англ. - М.: Медицина, 1980.
1. Банкл Г. Врожденные пороки сердца и крупных сосудов: Пер. с англ. - М.: Медицина, 1980. 2. Беришвили И.И., Рагимов Ф.Р., Лебедева Т.М., Вахромеева М.Н. Анатомические критерии отхождения аорты и легочной артерии от правого желудочка // Арх. пат. - 1990 - № 5. - С. 21-27.
2. Беришвили И.И., Рагимов Ф.Р., Лебедева Т.М., Вахромеева М.Н. Анатомические критерии отхождения аорты и легочной артерии от правого желудочка // Арх. пат. - 1990 - № 5. - С. 21-27.  3. Бокерия Л.А., Гудкова Р.Г. Сердечно-сосудистая хирургия - 2015. Болезни и врожденные аномалии системы кровообращения. - М.: НЦССХ им. А.Н.Бакулева, 2016. - 208 с.
3. Бокерия Л.А., Гудкова Р.Г. Сердечно-сосудистая хирургия - 2015. Болезни и врожденные аномалии системы кровообращения. - М.: НЦССХ им. А.Н.Бакулева, 2016. - 208 с.  4. Клинические рекомендации. Двойное отхождение сосудов от правого желудочка. - 2016. - 25 c. Режим доступа: https://racvs.ru/clinic/files/2016/Double-passage.pdf (Дата обращения 24.01.2021).
4. Клинические рекомендации. Двойное отхождение сосудов от правого желудочка. - 2016. - 25 c. Режим доступа: https://racvs.ru/clinic/files/2016/Double-passage.pdf (Дата обращения 24.01.2021). 5. Петренко Ю.В., Ляпунова А. А., Федосеева Т. А., Мызникова И. В. Клинические рекомендации. Диагностика и тактика ведения врожденных пороков сердца в неонатальном периоде. - 2016 - 31 c. Режим доступа: https://www.mrckb.ru/files/VPS.pdf (Дата обращения 24.01.2021).
5. Петренко Ю.В., Ляпунова А. А., Федосеева Т. А., Мызникова И. В. Клинические рекомендации. Диагностика и тактика ведения врожденных пороков сердца в неонатальном периоде. - 2016 - 31 c. Режим доступа: https://www.mrckb.ru/files/VPS.pdf (Дата обращения 24.01.2021). 6. Саперова Е.В., Вахлова И.В. Врожденные пороки сердца у детей: распространенность, факторы риска, смертность // Вопросы современной педиатрии. - 2017. - Т. 16, № 2. - С. 126-133.
6. Саперова Е.В., Вахлова И.В. Врожденные пороки сердца у детей: распространенность, факторы риска, смертность // Вопросы современной педиатрии. - 2017. - Т. 16, № 2. - С. 126-133.  7. Bradley T.J., Karamlou T., Kulik A., Mitrovic B., Vigneswaran T., Jaffer S. et al. Determinants of repair type, reintervention, and mortality in 393 children with double-outlet right ventricle // J Thorac Cardiovasc Surg. - 2007. - Vol. 134. - P. 967-973
7. Bradley T.J., Karamlou T., Kulik A., Mitrovic B., Vigneswaran T., Jaffer S. et al. Determinants of repair type, reintervention, and mortality in 393 children with double-outlet right ventricle // J Thorac Cardiovasc Surg. - 2007. - Vol. 134. - P. 967-973 8. Hoffman J.I.E. The natural and unnatural history of congenital heart disease Chichester: Wiley-Blackwell. - 2009.
8. Hoffman J.I.E. The natural and unnatural history of congenital heart disease Chichester: Wiley-Blackwell. - 2009. 9. Nakajima Y. Second lineage of heart forming region provides new understanding of conotruncal heart defects // Congenit Anom (Kyoto). - 2010. - Vol. 50. - P. 8-14.
9. Nakajima Y. Second lineage of heart forming region provides new understanding of conotruncal heart defects // Congenit Anom (Kyoto). - 2010. - Vol. 50. - P. 8-14.  10. Walters H.L. 3rd, Mavroudis C., Tchervenkov C.I., Jacobs J.P., Lacour-Gayet F., Jacobs M.L. Congenital Heart Surgery Nomenclature and Database Project: double outlet right ventricle // Ann Thorac Surg. - 2000. - Vol. 69, № 4. - P. 249-263.
10. Walters H.L. 3rd, Mavroudis C., Tchervenkov C.I., Jacobs J.P., Lacour-Gayet F., Jacobs M.L. Congenital Heart Surgery Nomenclature and Database Project: double outlet right ventricle // Ann Thorac Surg. - 2000. - Vol. 69, № 4. - P. 249-263.
 |
Главное меню |
 |
Заглавие |
 |
Введение |
 |
Материалы и методы |
 |
Результаты и обсуждение |
 |
Литература |
Оригинальная верстка  |
|
Телефон: (4212) 76-13-96
«Дальневосточный медицинский журнал»