2024 год № 4
Медико-биологические науки
1colobud@yandex.ru, https://orcid.org/0000-0002-6941-1997
2t.cherdantseva@rzgmu.ru, https://orcid.org/0000-0002-7292-4996
3budarev.v@yandex.ru, https://orcid.org/0000-0001-5517-0005
4shelvit94@gmail.com, https://orcid.org/0000-0003-2617-8707
Аннотация:
Ключевые слова:
1colobud@yandex.ru, https://orcid.org/0000-0002-6941-1997
2t.cherdantseva@rzgmu.ru, https://orcid.org/0000-0002-7292-4996
3budarev.v@yandex.ru, https://orcid.org/0000-0001-5517-0005
4shelvit94@gmail.com, https://orcid.org/0000-0003-2617-8707
Abstract:
Key words:
Введение |
 |
 |
Кровотечения из варикозно-расширенных вен пищевода - серьезная, не до конца решенная проблема [1]. К настоящему моменту разработано значительное количество различных, в том числе высокотехнологичных способов лечения таких больных. Однако их применение на высоте кровотечения зачастую затруднено ввиду тяжелого состояния пациента, проблем организационного плана, иногда - наличия прямых противопоказаний [2]. По факту, арсенал средств, доступных врачам ургентных хирургических отделений крайне ограничен. Указанные факты предопределяют актуальность поисковых работ, направленных на создание новых способов гемостаза, пригодных в данной клинической ситуации.
В то же время, разработчики новых лечебных методик неизбежно сталкиваются с серьезной проблемой. Апробация разработанных способов гемостаза на пациентах с продолжающимся кровотечением из вен пищевода крайне затруднительна [3]. Подвергать этих и без того находящихся в тяжелом состоянии больных дополнительной опасности из-за применения не доказавших свою эффективность методов лечения недопустимо. Отсюда напрашивается вывод: разработка и внедрение в клиническую практику новых способов остановки кровотечений из вен пищевода возможны только при наличии достоверной модели данного патологического состояния, позволяющей производить апробацию и объективную оценку методик без привлечения реальных больных.
Наиболее очевидным способом решения данной задачи является моделирование интересующего патологического состояния на лабораторном животном [4, 5]. Необходимо отметить, что количество исследований по моделированию у животных портальной гипертензии достаточно велико, они подробно описаны [6, 7]. А вот моделирование кровотечений из вен пищевода, развивающихся на фоне портальной гипертензии - на порядок менее изученная проблема. Более того, в сообщениях некоторых исследователей можно найти указание на неудачный опыт: формирование портальной гипертензии не обязательно приводит к необходимым изменениям в венах пищевода [8]. Подобрать технику эксперимента для получения нужного эффекта - сама по себе интересная научная задача, особенно если учесть, что дизайн исследования должен в правовом и этическом плане максимально соответствовать принципу "трех R" (Replacement - замена, Reduction - уменьшение, Refinement - уточнение) [9, 10].
Цель исследования: разработать пригодный для практического использования способ моделирования кровотечений из вен пищевода у лабораторных животных.
Материалы и методы
|
 |
 |
Основой исследования стали результаты экспериментальной работы, проведенной в операционной вивария Рязанского государственного медицинского университета с использованием имеющихся в нем стандартного набора хирургического инструментария и аппаратуры для обеспечения анестезиологического пособия.
Объектом исследования стали домашние свиньи породы Крупная белая в количестве 12 штук. Вес тел животных - 30-35 кг, все самки. К каждому животному прилагалось ветеринарное свидетельство, выданное ГБУ РО "Рязанская районная ветеринарная станция".
Анестезиологическое пособие осуществлялось в форме комбинированного наркоза, включающего внутримышечное введение препарата Золетил из расчета 1 мл/кг массы тела животного один раз в 40 минут, и ингаляцию препарата Севофлуран в смеси с кислородом в режиме спонтанного дыхания через специальная маску исходя из достижения минимальной альвеолярной концентрации равной 2-3.
Эвтаназия животного осуществлялась подачей инертного газа (азота). Данная методика была юридически закреплена документом Стандартная операционная процедура № 8 "Способы эвтаназии", утвержденным в Рязанском государственном медицинском университете 24.04.2018. Она полностью соответствовала Директиве 2010/63/EU Европейского парламента и совета Европейского союза по охране животных, используемых в научных целях.
Указанные выше способы проведения анестезиологического пособия и эвтаназии полностью соответствуют положениям упомянутого ранее принципа "трех R". Важными компонентами достижения этого соответствия стали также проводимая в послеоперационном периоде терапия (поддержание водно-электролитного баланса животного и детоксикация путем внутривенного капельного введения кристаллоидных растворов, внутримышечное ведение препарата Кеторол с целью обезболивания) и решение ограничить выборку 12 животными. К сожалению, выполнить пункт Replacement (замена) в рамках нашего исследования было невозможно.
Необходимые в рамках проводимого исследования эндоскопические манипуляции выполнялись с помощью фиброгастроскопа Olympus GIF type E и биопсийных щипцов Olympus FB-25K-1 с круглыми браншами без иглы.
На этапе проверки функциональности модели были задействованы зонды-обтураторы Сенгстакена-Блэкмора Зо-ОЗРИ Тип 1 № 23 длиной 800 мм.
Полученный в ходе работы биопсийный материал исследовался на кафедре гистологии, патологической анатомии и медицинской генетики Рязанского государственного медицинского университета. Препараты окрашивались по Ван Гизону, гематоксилином и эозином, исследовались при 100- и 200-кратном увеличении с помощью микроскопа "Leica DM2000" ("Leica Мicrosystems", Германия) Морфометрия и обработка данных выполнялись при помощи программ ImageJ (США) и Microsoft Excel 2016 (США) соответственно.
Ряд количественно оцененных во время исследования параметров был подвергнут статистической обработке, производился расчет t-критерия Стьюдента для независимых выборок.
Результаты и обсуждение
|
 |
 |
Среди всего разнообразия используемых лабораторных животных практически единственным реальным кандидатом для моделирования кровотечений из вен пищевода является домашняя свинья. Это животное достаточно доступно, относительно дешево, имеет очень высокую степень сходства с анатомией и физиологией человека. Принципиально важно, что по размерам и пропорциям тела свинья также близка к человеку, что позволяет использовать те же инструменты, приборы и изделия, что и при работе с реальным больным.
Для получения модели кровотечения из вен пищевода в организме животного на первом этапе оперативным путем формировалась портальная гипертензия, на втором этапе производилось механическое повреждение вены в пищеводе.
Формирование у свиньи портальной гипертензии достигалось дозированным сдавлением элементов печеночно-двенадцатиперстной связки пластиковым хомутом с многопозиционной защелкой. Данная методика была отработана нами ранее и защищена патентом на изобретение № 2770735 от 21.04.22. Суть проводимой операции заключалась в том, что после выполнения верхнесрединной лапаротомии пластиковый хомут проводился вокруг печеночно-двенадцатиперстной связки и замыкался в кольцо, охватывая все ее элементы кроме заранее выделенного холедоха. Постепенное затягивание хомута приводило к частичному сдавлению сосудов (как печеночной артерии, так и ветвей воротной вены). Поскольку организм свиньи очень быстро начинает реагировать на нарушение кровоснабжения печени, возникала тахикардия. Именно она была использована как количественный признак достаточной степени затягивания хомута. Эмпирическим путем было установлено, что перемещение защелки необходимо прекращать, когда частота сердечных сокращений животного превысила исходную на 30 %.
Необходимо отметить, что примененный нами метод формирования внепеченочной портальной гипертензии сильно отличается от используемой большинством исследователей дозированной перевязки воротной вены на игле [11]. Дело в том, что указанный способ удобен для работы на крысах и некоторых других животных, но плохо подходит для организма свиньи ввиду выраженного дольчатого строения печени, малой длины основного ствола воротной вены, значительного разброса диаметра сосудов даже в пределах однородной по размерам группы животных. Примененное нами воздействие на организм животного являлось более грубым, однако именно это позволяло надеяться на быстрое формирование в пищеводе изменений, необходимых для моделирования кровотечения. Решить поставленную задачу по-другому не представлялось возможным.
Второй этап моделирования начинался на четвертые сутки после первичной операции. Выбор этого момента обусловлен двумя причинами. С одной стороны, более раннее моделирование было бы невозможно, так как портокавальные анастомозы просто не успели бы раскрыться в необходимой степени, это подтверждается литературными данными [7]. С другой стороны, дизайн исследования не позволял осуществлять более длительное ожидание органических изменений в пищеводе. Ввиду выполнения достаточно грубого вмешательства в кровоснабжение внутренних органов была высока вероятность просто не успеть провести моделирование из-за гибели лабораторного животного.
На четвертые сутки после первой операции свинья бралась в операционную, погружалась в наркоз. С целью контроля состояния органов брюшной полости выполнялась релапаротомия. При этом визуально определялись признаки портальной гипертензии - асцит, полнокровие селезенки. Указанный этап исследования носил вспомогательный характер. Основной манипуляцией было выполнение фиброэзофагоскопии. Данная процедура представлена на рисунке 1. При этом выявлялось полнокровие вен пищевода, напоминающее варикозное расширение I-II степени по Шерцингеру. Типичной картиной было обнаружение в нижней трети пищевода 3-4 хорошо различимых венозных стволов диаметром 1-2 мм на фоне густой сети более мелких вен (рис. 2). Именно эти стволы и становились целью для дальнейших манипуляций.
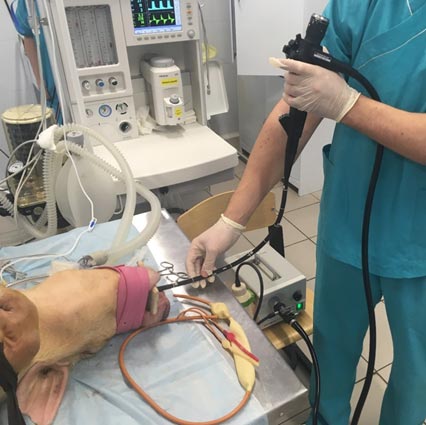
Рис. 1. Выполнение фиброэзофагоскопии лабораторному животному
Необходимо признать, что успешность первого этапа моделирования не была абсолютной. В 10 из 12 случаев (83,3 %) нужные изменения в организме животного были достигнуты, однако в 2 случаях (16,7 %) пищевод был интактен. Анализ этих ситуаций показал, что во время выполнения первичной операции были допущены отклонения от избранной технологии: в одном случае хомут не был затянут в достаточной степени, в другом - печеночно-двенадцатиперстная связка была взята в петлю хомута лишь частично.
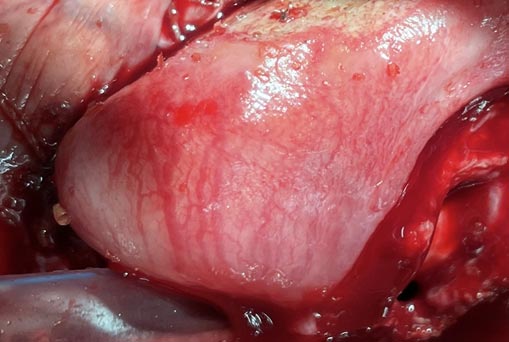
Рис. 2. Внутренняя поверхность нижней трети пищевода лабораторного животного на 4-е сутки после операции по формированию портальной гипертензии
На животных, у которых при фиброэзофагоскопии выявлялось венозное полнокровие (их было 10 штук), работа была продолжена. Визуально определялся самый крупный по размеру венозный ствол. Через инструментальный канал эндоскопа заводились биопсийные щипцы. Дальнейшее их использование полностью соответствовало алгоритму при взятии щипковой биопсии. Вращением винтов эндоскопа рабочая часть щипцов устанавливалась в проекции интересующей вены, производился ее захват. Резким рывком инструмент отдергивался, при этом отщипывался фрагмент венозной стенки и начиналось кровотечение. На этом моделирование считалось законченным, появлялась возможность приступать к практическому использованию модели, остановке возникшего кровотечения тем или иным способом.
Важным аспектом исследования стало объективное подтверждение необходимых изменений в организме свиньи, что было важно для легитимизации модели. С этой целью из тел животных после их выведения из эксперимента изымался биопсийный материал - фрагменты стенки нижней трети пищевода. В качестве эталона для сравнения такой же материал был взят из свиней, не подвергавшихся каким-либо манипуляциям на гепатопанкреатобиллиарной зоне. Было отмечено, что подслизистая оболочка пищевода утолщена, содержит большое количество полнокровных вен с деформированными стенками. Обнаруженная картина представлена на рисунке 3. Было произведено морфометрическое исследование изготовленных микропрепаратов с помощью программы ImageJ (США). Данная программа позволяет автоматизировать процессы обработки изображений. С ее помощью на гистологических препаратах можно в ручном или автоматическом режиме выделить интересующие объекты, вычислить их площадь, статистические показатели пиксельных значений [12]. Проведенное исследование показало увеличение средней площади просвета вен подслизистой основы пищевода в 3,59 раза по сравнению с интактным пищеводом. Средняя площадь вены в контрольной группе была равна 7 460 мкм2 (максимальное значение - 9 528 мкм2, минимальное - 2 102 мкм2, количество измерений - 7), средняя площадь просвета вены при моделировании портальной гипертензии была равна 26 802 мкм2 (максимальное значение - 45 752 мкм2, минимальное - 10 382 мкм2, количество измерений - 7). Выявленные различия по площади вен подслизистой основы пищевода были статистически достоверны (tЭмп=4,7, tКр=3,05, p≤0,01).
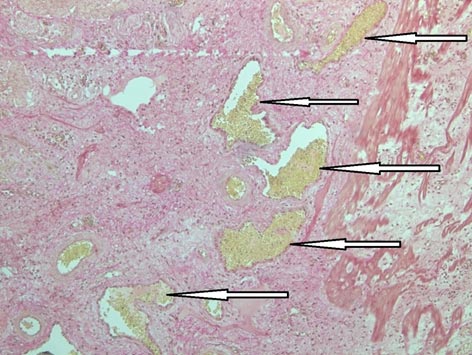
Рис. 3. Препарат пищевода свиньи при моделировании портальной гипертензии. Стрелками обозначены расширенные и полнокровные вены подслизистой оболочки. Окраска по Ван Гизону, 100-кратное увеличение
Проверкой функциональности полученных моделей кровотечения из вен пищевода можно считать тот факт, что 5 животным в финале эксперимента с гемостатической целью производилась установка стандартного зонда-обтуратора Сенгстакена-Блэкмора. Оценка эффективности работы данного изделия не проводилась, так как в этом не было необходимости. Главное то, что были продемонстрированы сама возможность введения в пищевод животного устройства, находящего повседневное применение в клинической практике, его штатное функционирование. Соответственно, это показало возможность будущего применения созданной модели для оценки других способов гемостаза.
Полученные результаты исследования нуждаются в обсуждении. Первый важный вопрос - достоверность созданной модели. Картина изменений в пищеводе животного по внешнему виду достаточно сильно отличается от того, что можно обнаружить при эндоскопии у пациента с портальной гипертензией. Дело в том, что варикозная трансформация вен пищевода - хронический, длительно текущий процесс, связанный со значительной перестройкой сосудистой стенки и дегенеративными процессами в ней. Получить такие же изменения в пищеводе животного за трое суток не представляется возможным. Однако, с нашей точки зрения, этого и не требуется. Вызвав венозное полнокровие в стенке пищевода, мы получили необходимый субстрат, доступный для повреждения биопсийными щипцами. При этом источник кровотечения выглядит непривычно, но на функциональность модели это не влияет.
Второй важный вопрос - универсальность созданной модели. Безусловно, она таковой не является. Утверждать, что разработанная модель кровотечения из вен пищевода позволяет отрабатывать любые методики гемостаза нельзя. В частности, она не применима для оценки медикаментозного лечения. Однако, если речь идет о локальном механическим, физическом или химическом воздействии на стенку пищевода со стороны его внутренней поверхности, создаваемые условия в высокой степени повторяют реальную клиническую ситуацию.
Выводы
|
 |
 |
1. Дозированное сдавление печеночно-двенадцатиперстной связки домашней свиньи пластиковым хомутом приводит к 4-м суткам послеоперационного периода к возникновению полнокровия вен пищевода, напоминающего варикозное расширение вен I-II степени.
2. Морфометрическое исследование гистологических препаратов с помощью программы ImageJ показывает, что пищевод домашней свиньи, подвергнутой дозированному сдавлению печеночно-двенадцатиперстной связки, к 4-м суткам послеоперационного периода характеризуется статистически достоверным увеличением средней площади просвета вен подслизистой основы в 3,59 раза по сравнению с интактным пищеводом.
3. В условиях эксперимента в 83,3 % случаев на базе организма домашней свиньи удалось создать модель кровотечения из вен пищевода путем дозированного сдавления печеночно-двенадцатиперстной связки пластиковым хомутом с последующим повреждением при фиброэзофагоскопии полнокровных вен пищевода биопсийными щипцами.
Список источников |
 |
 1. Юпатов Г.И., Прищепенко В.А. Алгоритм диагностики и дифференциальной диагностики хронических диффузных заболеваний печени (хронического гепатита и цирроза печени) в трудных клинических ситуациях, основанный на определении ферментативных активностей сыворотки крови // Наука молодых (Eruditio Juvenium). - 2020. - Т. 8, № 4. - С. 566-573.
1. Юпатов Г.И., Прищепенко В.А. Алгоритм диагностики и дифференциальной диагностики хронических диффузных заболеваний печени (хронического гепатита и цирроза печени) в трудных клинических ситуациях, основанный на определении ферментативных активностей сыворотки крови // Наука молодых (Eruditio Juvenium). - 2020. - Т. 8, № 4. - С. 566-573.  2. Стрижаков А.Н., Герадзe В.Н. Современное состояние проблемы цирроза печени // Российский журнал гастроэнтерологии, гепатологии, колопроктологии. - 2009. - Т. 1, № 2. - С. 87-88.
2. Стрижаков А.Н., Герадзe В.Н. Современное состояние проблемы цирроза печени // Российский журнал гастроэнтерологии, гепатологии, колопроктологии. - 2009. - Т. 1, № 2. - С. 87-88.  3. Königshofer P., Brusilovskaya K., Schwabl P., Reiberger T. Animal models of portal hypertension // Biochim Biophys Acta Mol Basis Dis. - 2019. - № 1865 (5). - P. 1019-1030.
3. Königshofer P., Brusilovskaya K., Schwabl P., Reiberger T. Animal models of portal hypertension // Biochim Biophys Acta Mol Basis Dis. - 2019. - № 1865 (5). - P. 1019-1030. 4. Bosch J., Iwakiri Y. The portal hypertension syndrome: etiology, classification, relevance, and animal models // Hepatol Int. - 2018. - № 12. - P. 1-10.
4. Bosch J., Iwakiri Y. The portal hypertension syndrome: etiology, classification, relevance, and animal models // Hepatol Int. - 2018. - № 12. - P. 1-10. 5. Nishida R., Inoue R., Takimoto Y., Hamashima H., Kita T. Endoscopic sclerotherapy in a rat model of esophageal varices // Scand J Gastroenterol. - 1995. - № 30 (5). - P. 489-496.
5. Nishida R., Inoue R., Takimoto Y., Hamashima H., Kita T. Endoscopic sclerotherapy in a rat model of esophageal varices // Scand J Gastroenterol. - 1995. - № 30 (5). - P. 489-496. 6. Гарбузенко Д.В. Экспериментальные методы изучения портальной гипертензии // Российский журнал гастроэнтерологии, гепатологии, колопроктологии. - 2010. - № 2. - С. 4-12.
6. Гарбузенко Д.В. Экспериментальные методы изучения портальной гипертензии // Российский журнал гастроэнтерологии, гепатологии, колопроктологии. - 2010. - № 2. - С. 4-12. 7. Евсеенко Д.А., Дундаров З.А., Надыров Э.А. Экспериментальная модель цирроза печени у лабораторных животных // Проблемы здоровья и экологии. - 2019. - № 1. - С. 72-77.
7. Евсеенко Д.А., Дундаров З.А., Надыров Э.А. Экспериментальная модель цирроза печени у лабораторных животных // Проблемы здоровья и экологии. - 2019. - № 1. - С. 72-77.  8. Maluf-Filho F., Meyer A., Martins P. Experimental model of portal hypertension and esophagogastric varices in minipigs: pressure and endoscopic pilot study // Acta Cir Bras. - 2022. - № 37 (1). - e370103.
8. Maluf-Filho F., Meyer A., Martins P. Experimental model of portal hypertension and esophagogastric varices in minipigs: pressure and endoscopic pilot study // Acta Cir Bras. - 2022. - № 37 (1). - e370103. 9. Липатов В.А., Крюков А.А., Северинов Д.А. Этические и правовые аспекты проведения экспериментальных биомедицинских исследований in vivo. Часть II // Российский медико-биологический вестник им. академика И.П. Павлова. - 2019. - Т. 27, № 2. - C. 245-257.
9. Липатов В.А., Крюков А.А., Северинов Д.А. Этические и правовые аспекты проведения экспериментальных биомедицинских исследований in vivo. Часть II // Российский медико-биологический вестник им. академика И.П. Павлова. - 2019. - Т. 27, № 2. - C. 245-257.  10. Russell W., Burch R. The principles of humane experimental technique // Methuen, London. - 1959. - 238 p.
10. Russell W., Burch R. The principles of humane experimental technique // Methuen, London. - 1959. - 238 p. 11. Арефьев Н.О., Гарбузенко Д.В. Выбор оптимальной методики частичного лигирования воротной вены при моделировании внепеченочной портальной гипертензии // Вестник Совета молодых ученых и специалистов Челябинской области. - 2016. - Т. 1, № 1. - С. 14-19.
11. Арефьев Н.О., Гарбузенко Д.В. Выбор оптимальной методики частичного лигирования воротной вены при моделировании внепеченочной портальной гипертензии // Вестник Совета молодых ученых и специалистов Челябинской области. - 2016. - Т. 1, № 1. - С. 14-19.  12. Мыцик А.В. Использование программы ImageJ для автоматической морфометрии в гистологических исследованиях // Омский научный вестник. - 2011. - № 2. - С. 187-189.
12. Мыцик А.В. Использование программы ImageJ для автоматической морфометрии в гистологических исследованиях // Омский научный вестник. - 2011. - № 2. - С. 187-189.
Телефон: (4212) 76-13-96
«Дальневосточный медицинский журнал»

