2024 год № 4
Медико-биологические науки
1m-i-s-h-e-l@mail.ru, https://orcid.org/0000-0002-7600-7992
2v-dav@mail.ru, https://orcid.org/0000-0002-4201-9661
3mdromanov@yandex.ru
5m-dav@list.ru, https://orcid.org/0009-0008-7270-6885
6chatkin_v@mail.ru, https://orcid.org/0000-0001-8652-0071
4Первый Московский государственный медицинский университет имени И.М. Сеченова Министерства здравоохранения Российской Федерации (Сеченовский Университет), Москва, Россия, bev-sechenov@mail.ru, https://orcid.org/0000-0001-9928-5234
Аннотация:
Ключевые слова:
1m-i-s-h-e-l@mail.ru, https://orcid.org/0000-0002-7600-7992
2v-dav@mail.ru, https://orcid.org/0000-0002-4201-9661
3mdromanov@yandex.ru
5m-dav@list.ru, https://orcid.org/0009-0008-7270-6885
6chatkin_v@mail.ru, https://orcid.org/0000-0001-8652-0071
4First Moscow State Medical University named after I.M. Sechenov Ministry of Health of the Russian Federation (Sechenov University), Moscow, Russia, bev-sechenov@mail.ru, https://orcid.org/0000-0001-9928-5234
Abstract:
Key words:
Введение |
 |
 |
Механическая желтуха - это распространенное осложнение заболеваний гепатопанкреатобилиарной системы, характеризуемое нарушением оттока желчи по желчевыводящим путям в двенадцатиперстную кишку из-за механических препятствий [1]. Учитывая, что смертность пациентов с данной патологии достигает 36 %, пациент должен в кротчайшие сроки получить необходимое лечение с целью профилактики развития острой декомпенсированной печеночной недостаточности [2]. Несмотря на широкое внедрение в билиарную хирургию инновационных малоинвазивных технологий, послеоперационная летальность больных с обтурационным холестазом до настоящего времени остается высокой и находится в пределах от 27 % до 35 % [3].
В настоящее время большое количество исследований указывают на значительную роль деструктивно-воспалительного процесса в патогенезе механической желтухи у пациентов в послеоперационном периоде, о чем свидетельствует развитие цитокинового дисбаланса [4]. Нарушение иммунного гомеостаза, в частности цитокинового статуса у больных с механической желтухой во многом определяют характер течения патологического процесса [5]. В связи с этим комплексное изучение содержания и баланса цитокинов на фоне механической желтухи и после восстановления пассажа желчи открывает доступ к пониманию молекулярно-клеточных предпосылок в изменении гомеостаза печеночной ткани и развитии послеоперационных осложнений. Понимание патогенеза острой печеночной недостаточности один из важнейших подходов к ее лечению, позволяющий эффективно использовать имеющиеся терапевтические подходы [6].
В настоящее время в литературных данных отсутствует информация о влиянии гепатопротекторов на состояние цитокинового баланса в ткани печени. Кроме того, в арсенале врачей, имеется небольшой спектр гепатопротекторов с доказанной эффективностью при механической желтухе. Поэтому, изучение влияния гепатопротекторов на динамику воспалительного баланса в печени способствует совершенствованию подходов к лечению пациентов с данной патологией.
Материалы и методы
|
 |
 |
Предметом исследования явился 2-аминоэтансульфонат магния (получивший шифр разработчика ЛБК-527), разработанный в АО "ВНЦ БАВ" (Россия) под руководством д.х.н., профессора С.Я. Скачиловой, предложенного в качестве перспективного химического соединения с возможной гепатопротекторной активностью. В качестве препарата сравнения использовали S-аденозил-L-метионин (коммерческое название "Гептрал" компания "ABBOTT" (США).
Эксперименты были выполнены на 250 белых нелинейных крысах обоего пола, разделенных на 5 групп. Группу № 1 составили интактные животные (n=10), группу № 2 - ложнооперированные (n=60), группу № 3 - животные с обратимой механической желтухой без медикаментозной коррекции (n=60), группу № 4 - животные с обратимой механической желтухой на фоне введения 2-аминоэтансульфона магния (n=60), группу № 5 - животные с обратимой механической желтухой на фоне введения S-аденозил-L-метионина (n=60).
Протоколы лабораторных экспериментов прошли этическую экспертизу на заседании Локального этического комитета Медицинского института ФГБОУ ВО "МГУ им. Н.П. Огарева (01.10.2021 года, протокол № 99).
В качестве обезболивания во время проведения хирургических вмешательств использовано внутрибрюшинное введение водного раствора "Золетил 100,0" (VIRBAC (Франция)) в дозе 20 мг/кг + "Ксила" (Interchemiewerken De Adelaar, B.V., Нидерланды) в дозировке 1,2 мл/кг.
Для формирования обратимого холестаза использовали оригинальный способ, разработанный авторами "Способ формирования обратимой механической желтухи" [7]. Продолжительность окклюзии составила 5 суток, после чего восстанавливали пассаж желчи. В группе ложнооперированных животных выполняли срединную лапаротомию, осуществляли доступ к холедоху и брыжейке двенадцатиперстной кишки, после чего послойно ушивали лапаротомную рану.
После ликвидации билиарной окклюзии животным, получавшим исследуемую субстанцию, ежесуточно в хвостовую вену вводили водный раствор 2-аминоэтансульфоната магния в дозе 28 мг/кг в объеме 0,4 мл. Животным из группы сравнения внутривенно вводили адеметионин в дозе 60 мг/кг в объеме 0,4 мл. В качестве растворителя использовали 0,9 % раствор хлорида натрия. Животным без лечения и ложнооперированным крысам ежесуточно внутривенно вводили эквивалентный объем изотонического раствора хлорида натрия.
Продолжительность эксперимента после ликвидации механической желтухи и восстановления пассажа желчи составила 21 день. На 1, 3, 7, 14 и 21 сутки после восстановления пассажа желчи из эксперимента выводили по 6 животных с последующим извлечением печени для исследования. Для приготовления гомогената печени использовали 100 мг ткани, которую гомогенизировали в ступке с добавлением 1 мл фосфатно-щелочного буферного раствора (pH 7,4).
После получения гомогената осуществляли его экспозицию при температуре -20 °С на протяжении 12 час. При помощи двукратной смены циклов разморозки и заморозки происходило разрушение клеточных мембран. Следующим этапом производили центрифугирование полученных гомогенатов со скоростью 5 000 g, при температуре от 2 до 8 °С на протяжении 5 минут. Таким образом был получен супернатант, который отделяли и использовали для определения концентрации исследуемых про- и противовоспалительных цитокинов (рис. 1).
Рис. 1. Супернатанты печеночного гомогената для ИФА
Иммуноферментный анализ и изучение тканевой концентрации провоспалительных (ФНО-альфа, ИЛ-1) и противовоспалительных (ИЛ-10) цитокинов проводили с помощью медицинского лабораторного фотометра Stat Fax на кафедре госпитальной хирургии с курсами травматологии и ортопедии, офтальмологии Медицинского института ФГБОУ ВО "МГУ им. Н.П. Огарева".
При статистической обработке данных использован дисперсионный анализ (ANOVA) для определения наличия или отсутствия статистически значимой разницы между средними значениями трех или более независимых групп с использованием критерия Даннета.
Результаты и обсуждение
|
 |
 |
Результаты исследования представлены на рисунках 2, 3, 4, 5.
Концентрация про- и противовоспалительных цитокинов в исследуемых лечебных группах на 1 сутки после восстановления пассажа желчи практически не отличалась от контрольных значений. В динамике на 3 сутки после восстановления тока желчи в группе контроля отмечался рост ИЛ-1 и ФНО-альфа на 4 % и 21 % соответственно, что свидетельствовало о прогрессировании воспалительного процесса, тогда как на фоне введения ЛБК-527 и S-аденозил-L-метионина наблюдалось снижение ИЛ-1 и ФНО-альфа на 15 % и 44 % соответственно (рис. 3, 4).
Кроме того, у животных на фоне лечения рост ИЛ-10 составил 17 % в группе ЛБК-527 и 22 % в группе сравнения, тогда как у контрольных животных рост данного показателя составил всего лишь 4 % (рис. 5).
На 7 сутки после восстановления пассажа желчи концентрация ИЛ-1 в группе контроля была выше чем у интактных животных, однако, статистически не отличалась от аналогичного показателя у животных на фоне лечения. Несмотря на восстановление пассажа желчи у животных группы контроля концентрация ФНО-альфа была статистически значимо выше на протяжении всего эксперимента, тогда как на фоне введения исследуемой субстанции и препарата сравнения нормализация уровня данного показателя отмечалась уже к 14 суткам эксперимента (рис. 4). У животных на фоне введения ЛБК-527 и препарата сравнения на 7 сутки после восстановления желчеоттока отмечался рост ИЛ-10, который был статистически значимо выше в сравнении с группой контроля и с интактными животными и достигал 133,85±5,5 пг/мл и 139,7±9,1 пг/мл соответственно (рис. 5). Начиная с 14 суток отмечалась нормализация уровня противовоспалительных цитокинов во всех исследуемых группах.

Рис. 2. Концентрация некоторых про- и противовоспалительных цитокинов в гомогенате печени интактных и ложнооперированных животных
<
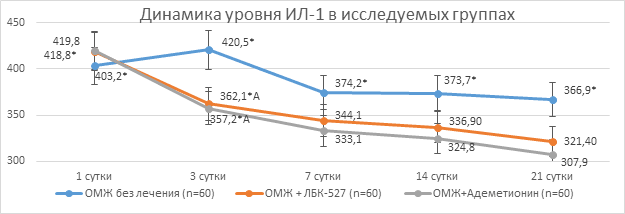
Рис. 3. Динамика концентрации Интерлейкина-1 в гомогенате печени при остром холестатическом повреждении на фоне восстановления пассажа желчи, при введении 2-аминоэтансульфоната магния и S-аденозил-L-метионина
Примечание. * - различия при сравнении с интактными крысами статистически достоверны при р<0,05 (одномерный дисперсионный анализ, критерий Даннета); А - различия при сравнении с группой ОМЖ без лечения статистически достоверны при р<0,05 (одномерный дисперсионный анализ, критерий Даннета).
Рис. 4. Динамика концентрации ФНО-альфа в гомогенате печени при остром холестатическом повреждении на фоне восстановления пассажа желчи, при введении 2-аминоэтансульфоната магния и S-аденозил-L-метионина
Примечание. * - различия при сравнении с интактными крысами статистически достоверны при р <0,05 (одномерный дисперсионный анализ, критерий Даннета); А - различия при сравнении с группой ОМЖ без лечения статистически достоверны при р<0,05 (одномерный дисперсионный анализ, критерий Даннета).
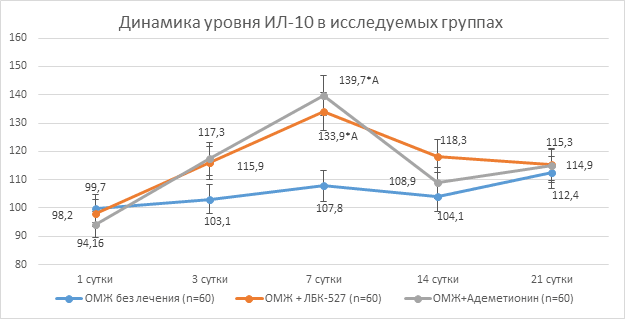
Рис. 5. Динамика концентрации Интерлейкина-10 в гомогенате печени при остром холестатическом повреждении на фоне восстановления пассажа желчи, при введении 2-аминоэтансульфоната магния и S-аденозил-L-метионина
Примечание. * - различия при сравнении с интактными крысами статистически достоверны при р <0,05 (одномерный дисперсионный анализ, критерий Даннета); А - различия при сравнении с группой ОМЖ без лечения статистически достоверны при р<0,05 (одномерный дисперсионный анализ, критерий Даннета).
К 21 суткам эксперимента в группе контроля несмотря на снижение уровня провоспалительных цитокинов их значение было статистически значимо выше чем у интактных животных (рис. 3, 4). В группах животных, получавших 2-аминоэтансульфонат магния и адеметионин, к 14 дню эксперимента концентрация всех исследуемых регуляторных молекул статистически не отличалась от таковой у интактных животных.
Интерлейкин-1, как медиатор воспаления при восстановлении пассажа желчи в двенадцатиперстную кишку сопровождается увеличением концентрации 3 суткам. Это указывает на продолжение альтерационных процессов, по-видимому вследствие, реперфузионного синдрома на фоне билиарной декомпрессии. Именно в этот период в клинической практике отмечается усиление печеночной недостаточности. На фоне приема адеметионина и ЛБК-527, наоборот, наблюдается выраженное снижение экспрессии интерлейкина-1, что говорит о быстром наступлении эффекта от применяемых фармакологических агентов, которые показывают высокую гепатопротекторную активность. На 7, 14, 21 сутки эта динамика сохраняется, и оба препарата в сравнительном аспекте действуют аналогично, не имея при этом достоверных различий в эффективности гепатопротекторной активности.
Таким образом, механическая желтуха сопровождается выраженным сдвигом цитокинового профиля в сторону провоспалительных регуляторных молекул. Использование 2-аминоэтансульфоната магния и S-аденозил-L-метионина в равной степени способствовало снижению выраженности воспаления в паренхиме печени, что отражалось в снижении экспрессии про-, и увеличением продукции противовоспалительных цитокинов.
Выводы
|
 |
 |
1. Окклюзия желчных протоков сопровождается смещением воспалительного баланса в сторону провоспалительных цитокинов. Несмотря на восстановление пассажа желчи в первые трое суток отмечается сохранение отрицательной воспалительной динамики в виде увеличения концентрации воспалительных иммунных триггеров на фоне относительной недостаточности противовоспалительных цитокинов. Начиная с 7 суток после восстановления пассажа желчи несмотря на медленное снижение воспалительной реакции в ткани печени уровень ФНО-альфа и ИЛ-1 остается статистически значимо выше чем в группе интактных животных на протяжении всего эксперимента.
2. Внутривенное введение 2-аминоэтансульфоната магния и адеметионина сопровождается сопоставимым гепатопротекторным эффектом, о чем свидетельствует сокращение сроков нормализации уровней интерлейкина-1 к 7 суткам, ФНО-альфа к 14 суткам, а также статистически значимым увеличением уровня противовоспалительного цитокина ИЛ-10 к 7 суткам после декомпрессии желчевыводящих путей.
Список источников |
 |
 1. Стяжкина С.Н., Хурамова Ю.Т., Короткова В.П. Анализ динамики и лечения механической желтухи по данным хирургической клиники // StudNet. - 2022. - Т. 5, № 5. - С. 4314-4329.
1. Стяжкина С.Н., Хурамова Ю.Т., Короткова В.П. Анализ динамики и лечения механической желтухи по данным хирургической клиники // StudNet. - 2022. - Т. 5, № 5. - С. 4314-4329. 2. Makhmudova G.F., Nurboboyev A.U. Treatment of mechanical jaundice via the modern way // Scientific progress. - 2021. - Vol. 2, № 6. - P. 530-537.
2. Makhmudova G.F., Nurboboyev A.U. Treatment of mechanical jaundice via the modern way // Scientific progress. - 2021. - Vol. 2, № 6. - P. 530-537.  3. Вебер В.Р., Кашаева М.Д., Прошин А.В., Швецов Д.А., Дубовая Т.К., Буйкин С.В., Бочкарева А.Н. Значение лимфодренирующих операций в комплексном лечении неопухолевых механических желтух // Вестник НовГУ. - 2023. - Т. 2, № 131. - С. 302-311.
3. Вебер В.Р., Кашаева М.Д., Прошин А.В., Швецов Д.А., Дубовая Т.К., Буйкин С.В., Бочкарева А.Н. Значение лимфодренирующих операций в комплексном лечении неопухолевых механических желтух // Вестник НовГУ. - 2023. - Т. 2, № 131. - С. 302-311. 4. Смирнова О.В., Елманова Н.Г. Роль цитокинов в патогенезе инфекционных осложнений при хирургическом лечении механической желтухи желчнокаменного генеза // Бюллетень сибирской медицины. - 2021. - Т. 20, № 3. - С. 105-111.
4. Смирнова О.В., Елманова Н.Г. Роль цитокинов в патогенезе инфекционных осложнений при хирургическом лечении механической желтухи желчнокаменного генеза // Бюллетень сибирской медицины. - 2021. - Т. 20, № 3. - С. 105-111. 5. Гаджиев Д.Н., Тагиев Э. Г., Гаджиев Н. Д. Состояние цитокинового статуса у больных с механической желтухой доброкачественного генеза // Хирургия. Журнал им. Н.И. Пирогова. - 2015. - № 5. - С. 56-58.
5. Гаджиев Д.Н., Тагиев Э. Г., Гаджиев Н. Д. Состояние цитокинового статуса у больных с механической желтухой доброкачественного генеза // Хирургия. Журнал им. Н.И. Пирогова. - 2015. - № 5. - С. 56-58.  6. Фомин А.М. Влияние селективной плазмосорбции на эндотоксикоз и цитокинемию при механической желтухе // Вестник анестезиологии и реаниматологии. - 2021. - Т. 18, № 5. - С. 40-46.
6. Фомин А.М. Влияние селективной плазмосорбции на эндотоксикоз и цитокинемию при механической желтухе // Вестник анестезиологии и реаниматологии. - 2021. - Т. 18, № 5. - С. 40-46. 7. Морозов М.А., Блинова Е.В., Давыдкин В.И., Морозова Н.И., Бородина Е.Н., Балашкина А.А. Способ формирования обратимой механической желтухи // Патент № 2785942. - 2021.
7. Морозов М.А., Блинова Е.В., Давыдкин В.И., Морозова Н.И., Бородина Е.Н., Балашкина А.А. Способ формирования обратимой механической желтухи // Патент № 2785942. - 2021.
Телефон: (4212) 76-13-96
«Дальневосточный медицинский журнал»

